多细胞模块化生物传感器开发框架-纽卡斯尔大学2017 iGEM项目简介
Posted iGEM
tags:
篇首语:本文由小常识网(cha138.com)小编为大家整理,主要介绍了多细胞模块化生物传感器开发框架-纽卡斯尔大学2017 iGEM项目简介相关的知识,希望对你有一定的参考价值。
纽卡斯尔大学2017年iGEM参赛队伍的基本信息:
iGEM比赛年度:2017年
队名:Newcastle
学校:纽卡斯尔大学(Newcastle University)
类别(Kind):大学生(Collegiate)
组别(Section):研究生组(Overgraduate)
地区:欧洲
国家:英国
领域/板块(track):基础研究进展(Foundational Advance)
纽卡斯尔大学2017年iGEM参赛队伍的获奖情况:
单项奖(Award):
最佳海报提名(Nominated for Best Poster)
最佳教育和公共参与提名(Nominated for Best Education & Public Engagement)
最佳部件收集提名(Nominated for Best Part Collection)
最佳检测项目的提名(Nominated for Best Measurement)
奖牌(Medal):金奖(Golden Medal)
项目名称:
Sensynova - a new era of biosensors
项目wiki:
http://2017.igem.org/Team:Newcastle
什么是生物传感器?
生物传感器可以被认为是能够通过使用生物组分(Turner,2013)来感测分析物(例如分子或化合物)或某些条件(例如pH或温度)的任何装置。 其中一个例子就是煤矿里的一只金丝雀,在一氧化碳的存在的情况下,金丝雀会死亡。 合成生物学家已经开发出一种更先进的生物传感器。 所有生物都使用本地生物传感装置来监测感兴趣的分子并启动细胞反应。 例如,细胞稳态的维持需要对金属,脂肪酸和过氧化氢等许多分子进行灵敏的检测和后续的调控(RensingæGrass,2003,ZhangæRock,2009 和 Marinho 等,2014)。双组分系统是细菌中常见的生物传感系统。 这些系统允许细菌通过在靶分子存在下传感器激酶的磷酸化对细胞外信号作出响应,随后磷酸化另外的响应调节蛋白。 这些反应调节因子可以通过蛋白质相互作用,转录调控或RNA结合来改变细胞行为(Gao等,2007)。
近年来,使用合成生物学方法生产的生物传感器的数量大幅增加。 合成生物学涉及工程原理在操纵生物系统中的应用。 使用这些方法构建的生物传感器适应先前讨论的天然细胞生物传感过程,例如蛋白质或RNA结合,并使用这些相互作用诱导报告基因如荧光蛋白的转录。
这些传感器可以表示为活的全细胞传感器,但也越来越多地在无细胞蛋白质合成系统中表达。 然而,迄今为止,这些系统的高昂成本还在限制它们在合成生物学中被更广泛使用(Smith等,2017)。
为什么生物传感器有用?

基于合成生物学的生物传感器的一个主要优势是其成本效益。 在研究阶段之后,生物传感器的生产仅依靠维持表达工程系统的细胞群,与其他传统方法如免疫测定或质谱法相比,这是一个相对便宜的过程。 合成生物传感器可以设计成不依赖额外的设备,这不仅增加了成本效益,而且还可以进行现场诊断(BhatiaČChugh,2013)。 合成生物学方法还可以将更复杂的行为引入生物传感器设计中,例如允许响应各种同时触发信号生成的逻辑门(Chappel & Freemont,2011)。
生物传感器的一个具体例子是由Aleksic等人开发的砷生物传感器。 ( 2007年 ) 。 这种传感器能够响应饮用水中砷的存在而产生pH变化。 在这个系统中,砷反应转录因子ArsR在没有砷的情况下抑制了pArs启动子。 当砷存在并与ArsR结合时,蛋白质不再结合并抑制启动子,使下游基因的转录成为可能。 在这个例子中,下游基因是脲酶,其产生可检测的pH变化。 因此,通过监测pH可以检测到砷的存在。
生物传感器开发人员面临什么问题?

纽卡斯尔大学团队的项目侧重于生物传感器开发的挑战:如果合成生物传感器比替代品好得多,而替代品通常昂贵且不能现场诊断,为什么它们的使用不能更加的广泛? 为了回答这个问题,项目团队向生物传感器开发方面的各个利益相关者咨询:从合成生物学领域内外,从早期研究阶段到最终用户。 他们通过skypy,通过电子邮件,出席会议。 确定了生物传感器开发者面临的问题在5个主要领域,下面详述。
部分可重用性
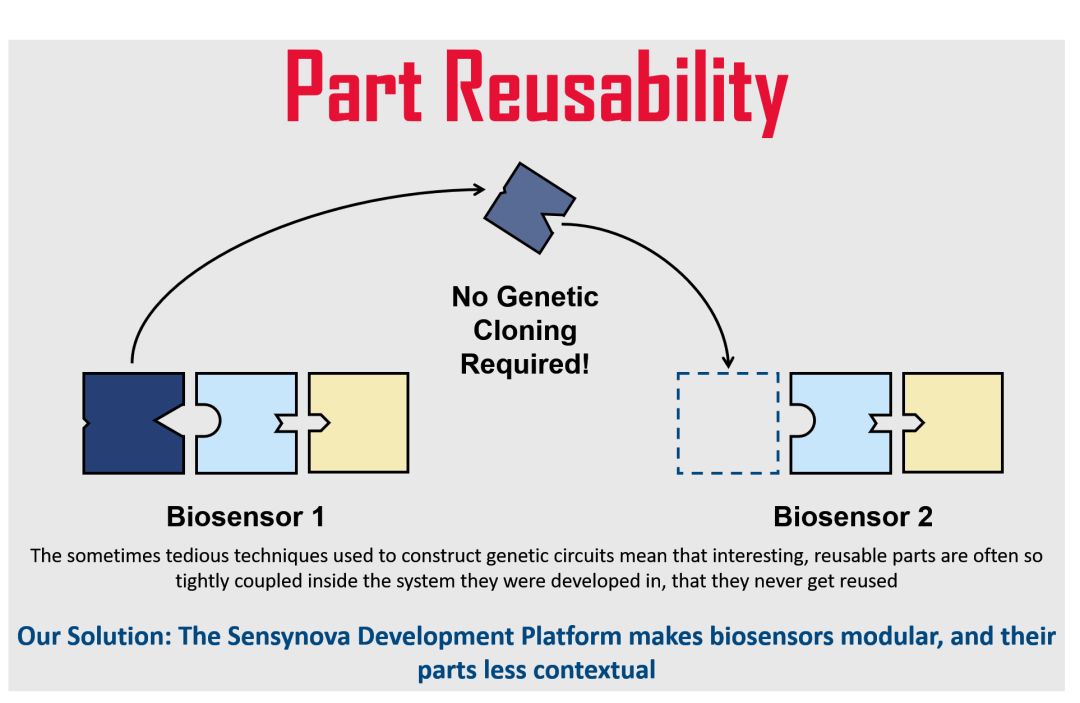
广泛的优化
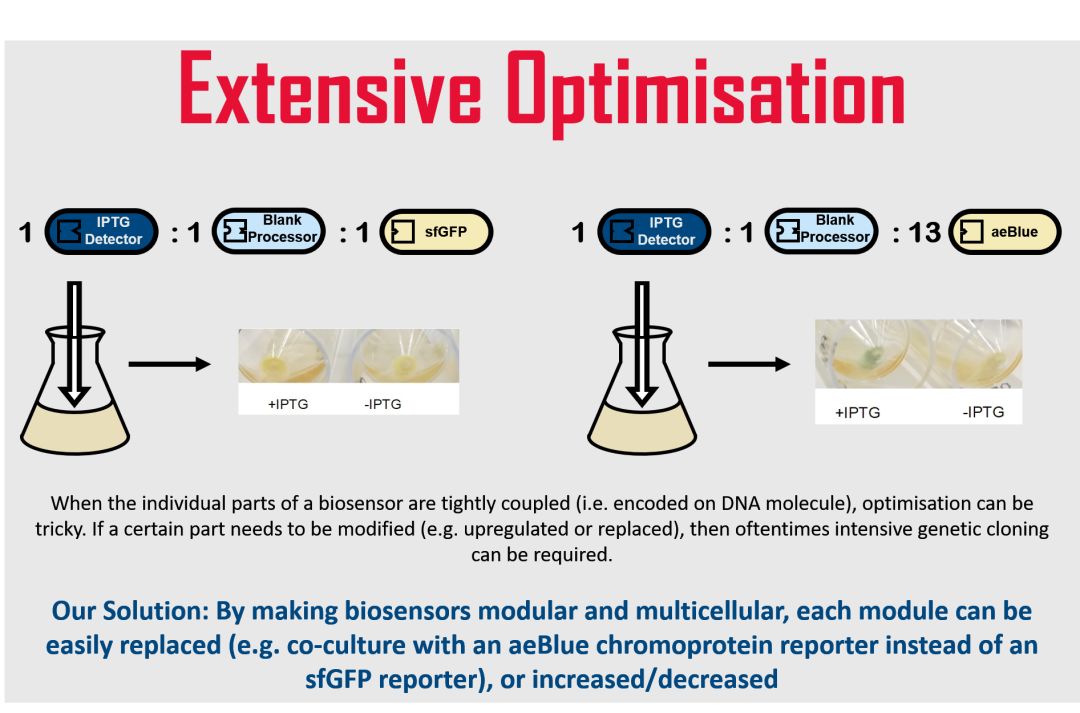
分析物范围扩展
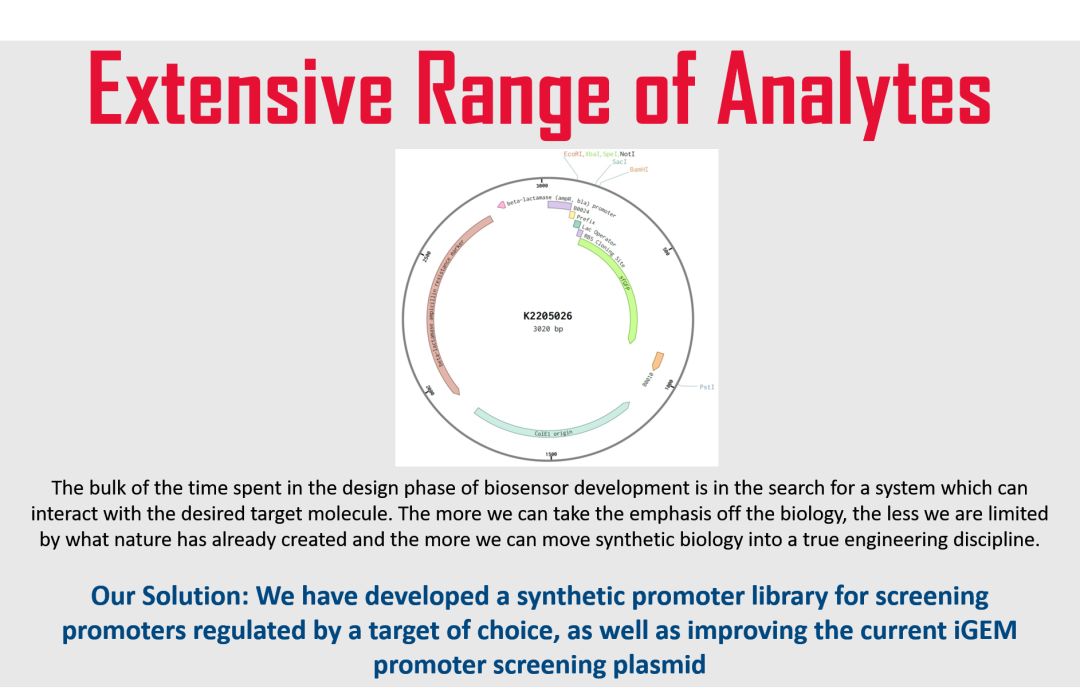
技术的吸收

GMO立法
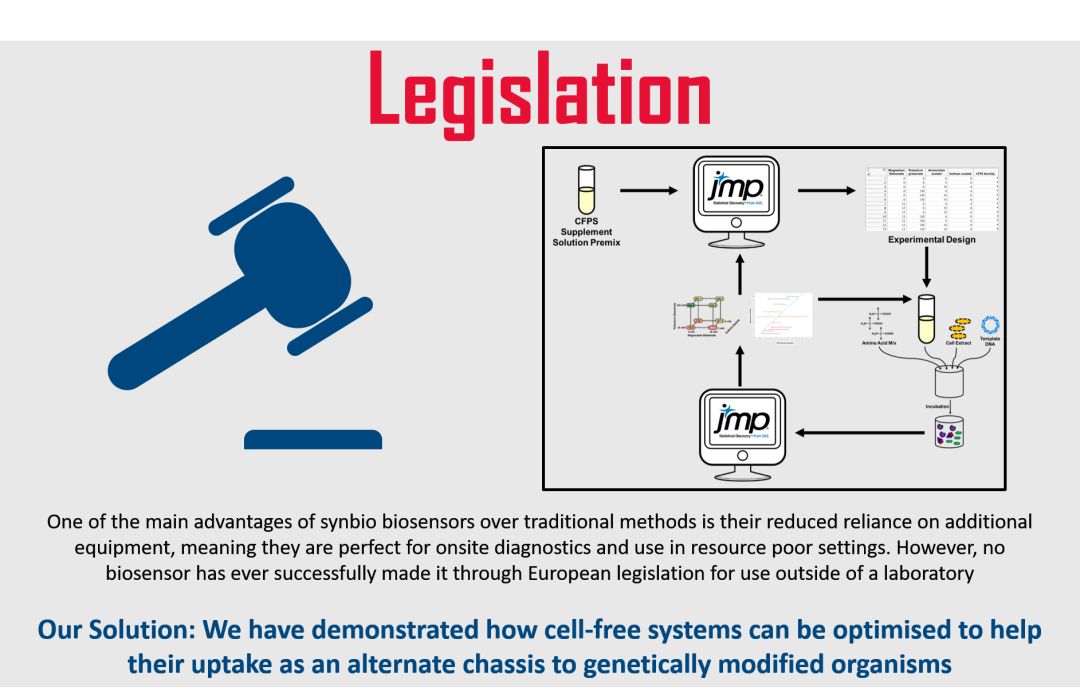
关于Sensynova框架
纽卡斯尔大学团队在这个项目中,提出了模块化设计的思路,其可以通过将生物传感器的组件分成不同的细胞进行通信以协调响应来改进模块性,并因此能够在没有进一步基因工程的情况下使用“现成的”部件。 正交群体感应系统Rhl和Las将被用作生物“导线”,将不同的生物传感器组件连接在一起。 组件的这种分离将使非特定组件与特定检测系统脱钩成为可能。 使用这种方法,生物传感器变体的生产将不需要后续的工程步骤:包含所需组分的细胞将被简单地混合在一起。
多细胞系统
生物传感器组件分解成单独的细胞可能具有很多除了易于生产外的额外的优点。 Goni-Moreno等人 (2011)曾经提出使用合成的群体感应电路使得每个细胞被认为是一个独立的逻辑门,这可以纠正在某些生物传感器中看到的“模糊逻辑”,其中随机细胞过程可能产生假阳性结果。 将生物传感器分成单独的细胞的另一个优点是它减少了任何一种细胞的负载。 如果需要一个细胞在高拷贝数的质粒如pSB1C3上表达整个生物传感器系统,则细胞中的资源可能变得有限,并且细胞生长速率可能成为问题。 通过将网络分成三分之一并在不同的细胞部件中表达它们,则不需要只要一种细胞来处理这种压力水平。
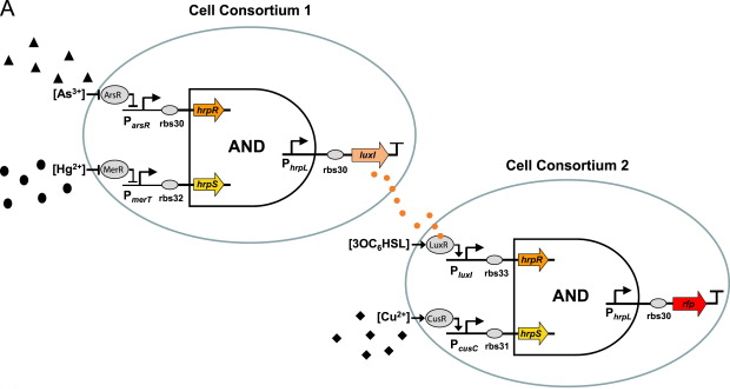
图1:Wang等人的三输入多细胞生物传感器设计。RFP是在砷,汞和铜的存在下生产的。 图片来自原文献。
Wang和他的同事在(2013)中描述了多细胞环境中生物传感器的概念。 Wang和其同事在多个细胞中使用遗传逻辑门将来自多个分析物检测的信号整合到一个输出中。 他们用这个概念来设计一个三重输入的重金属生物传感器,它只有在汞,砷和铜同时存在下才产生一个信号(图1)。 群体中的一种细胞类型使用遗传“与”门来激活在砷和汞存在下的luxI表达。 LuxI合成感应分子3OC6HSL。 群体中的第二种细胞类型使用相同的遗传“与”门,在HSL和铜的存在下产生红色荧光蛋白(RFP)。
在这项研究中提出的这种方法可以用于设计易于定制和模块化的生物传感器。 虽然这种设计确实允许在一定程度上对生物传感器进行定制(例如PhrpL-rbs30-rfp构建体可以被PhrpL-rbs30-sfGFP构建体所取代),但是各个部分仍然紧密地连接在同一个DNA分子上,并且大部分电路仍然在同一种细胞内。 另外,这种设计只允许设计具有与门的生物传感器,并且不能在系统中增加额外的信号处理模块。 然而,这项研究表明,生物传感器多细胞和模块化的原则是可能的和有用的。
研究人员的这些前期工作为纽卡斯尔大学团队的项目提供了灵感。通过一系列现成的模块组件来扩展它们的概念,通过系统分析以前的配置来增强设计的分离,以及使用不同比例的细胞系统来优化传感器响应特性。 项目团队还在设计中纳入了无细胞系统的想法。
群体感应机制
在Sensynova框架中,采用了两个群体感应(QS)机制:LasIR系统和RhlIR系统。 这两个系统都是在革兰氏阴性菌中发现的基于酰基 - 高丝氨酸内酯(AHL)的系统; 特别是Las和Rhl系统在铜绿假单胞菌中是作为毒力因子的调控机制的特征(Pearson等,1997)。 图2显示了Las QS系统的机制。RHL系统的机制也是相同的,除了用RhlI(其产生C4-HSL代替C12-HSL)代替LasI,并且用RhlR代替LasR 被C4-HSL激活并激活PRhl启动子的转录)。
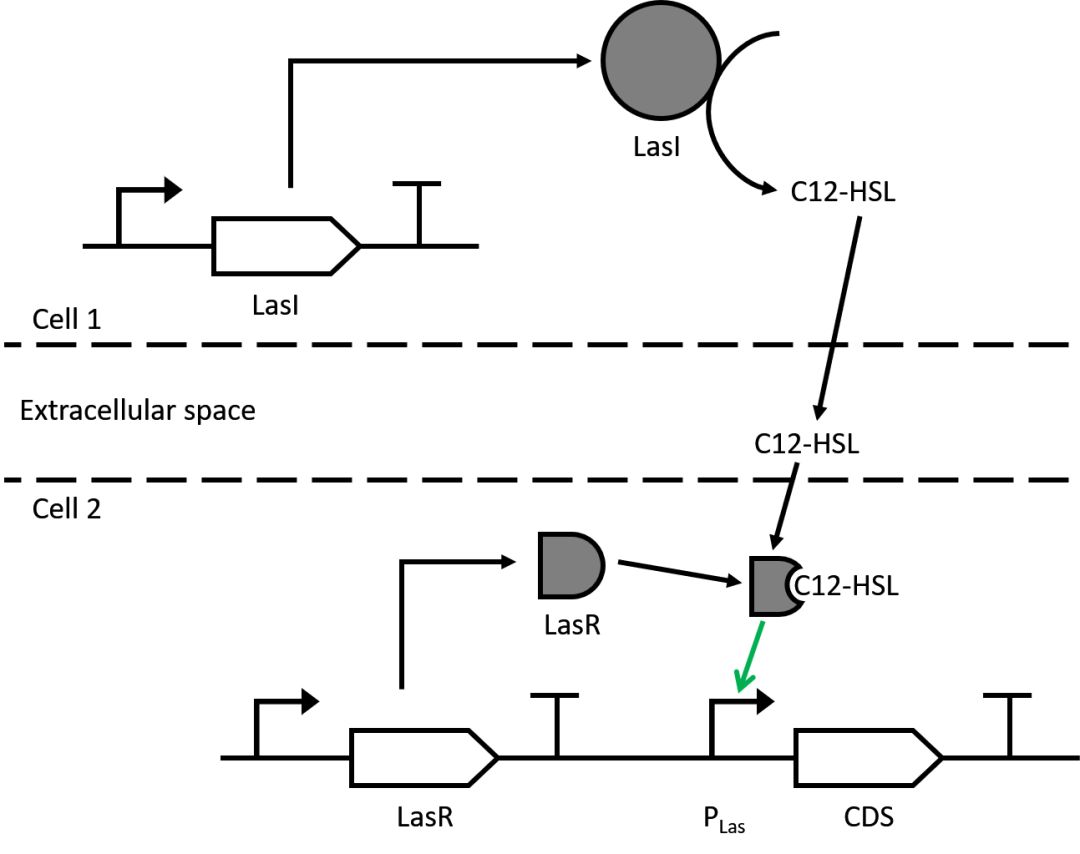
图2:LasIR群体感应机制。LasI是由一个细胞组成的。 LasI合成C12-HSL群体感应分子。 C12-HSL能够通过膜扩散到细胞外空间。 当在一个位置存在足够的LasI阳性细胞(产生LasI的细胞)时,细胞外空间中的C12-HSL的量达到阈值浓度。 此时,群体感应分子通过它们的膜扩散到周围的细胞中。 这些细胞也产生LasR转录因子。 C12-HSL可以与LasR结合,使转录因子能够从PLas启动子激活转录。
在自然界中,QS系统往往被病原体用作同步毒力因子生产的方法(Rutherford & Bassler,2012)。 当存在足够的病原体感染可能成功(由达到QS分子阈值所需的细胞量决定)时,表达由QS转录因子(例如LasR或Rh1R)调控的启动子控制下的毒力因子。 这使得产生协调的攻击,而不是单个或一小部分细胞产生毒力因子,表明他们的存在免疫系统,并减少成功感染的可能性。
QS机制提供了一种非常便利的机制来将细胞间通讯转化为合成的微生物群落。 群体中的一些细胞可以被设计成产生AHL合酶(例如,LasI或RhlI),而另一些细胞产生AHL转录因子(TF)(LasR或RhlR)。 然后可以在AHL-TF调控的启动子之后组装所需的部件,使得它们仅在发送细胞存在或激活时产生。 合成生物学中群体感应的一个例子是同步基因表达,这导致群体内变异性降低(Danino等人,2010)。
在Sensynova框架中,使用的群体感应机制如下。 lasR基因由受目标分析物/条件选择的启动子控制的检测细胞编码。 在靶标的存在下,产生LasR并合成C12-HSL并释放到细胞外空间。 LasR转录因子由处理细胞不断产生,当存在C12-HSL时,来自Plas启动子的转录被激活。 将期望的处理装置置于Plas启动子的控制下,并通过处理装置产生RhlI合酶。RhlI装置然后可以合成穿过细胞外空间的C4-AHL。 报道细胞编码并表达转录因子RhlR。 当处理细胞产生足够的C4-AHL时,AHL将通过膜进入群体的细胞中。 进入报道细胞的C4-AHL将与Rh1R结合,并激活来自报道基因的编码序列(例如超折叠GFP)上游的Prh1启动子的转录。 这个过程如图3所示。
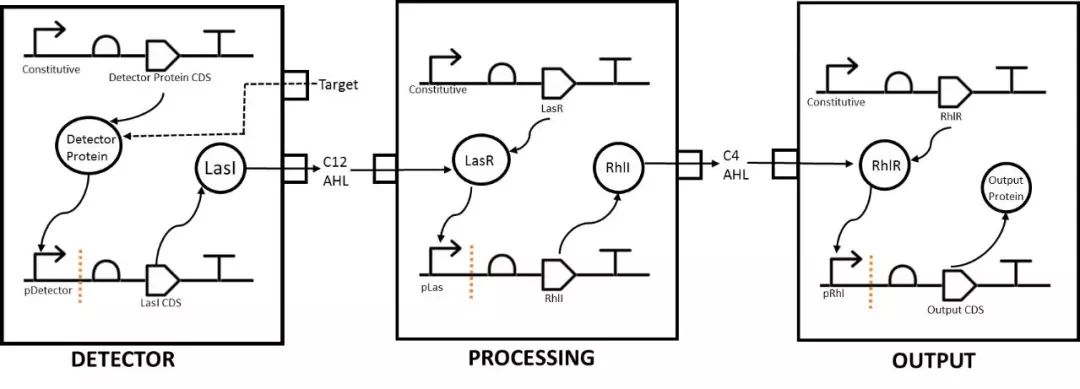
图3:Sensynova框架中的群体感应机制概述。
项目展望
现有生物传感器的设计仍存在诸多不足之处:如将复杂的基因电路导入同一种细胞导致的细胞代谢负担加重;同时由于是整体性的设计,要对电路进行微调和功能扩展时,需要重新设计并组装和导入。这让生物传感器在使用上非常不灵活。纽卡斯尔大学团队在本项目中提出了利用细胞间群体感应机制进行通信的多细胞模块化生物传感器设计框架。该框架旨在简化生物传感器开发的设计,实施和表征/优化阶段,为未来生物传感器的进一步开发指出了一条非常有潜力的路径,可能会开创生物传感器的一个崭新时代。

以上是关于多细胞模块化生物传感器开发框架-纽卡斯尔大学2017 iGEM项目简介的主要内容,如果未能解决你的问题,请参考以下文章