Thermodynamics---PV Diagram
Posted siranlee
tags:
篇首语:本文由小常识网(cha138.com)小编为大家整理,主要介绍了Thermodynamics---PV Diagram相关的知识,希望对你有一定的参考价值。
Thermodynamics---PV Diagram
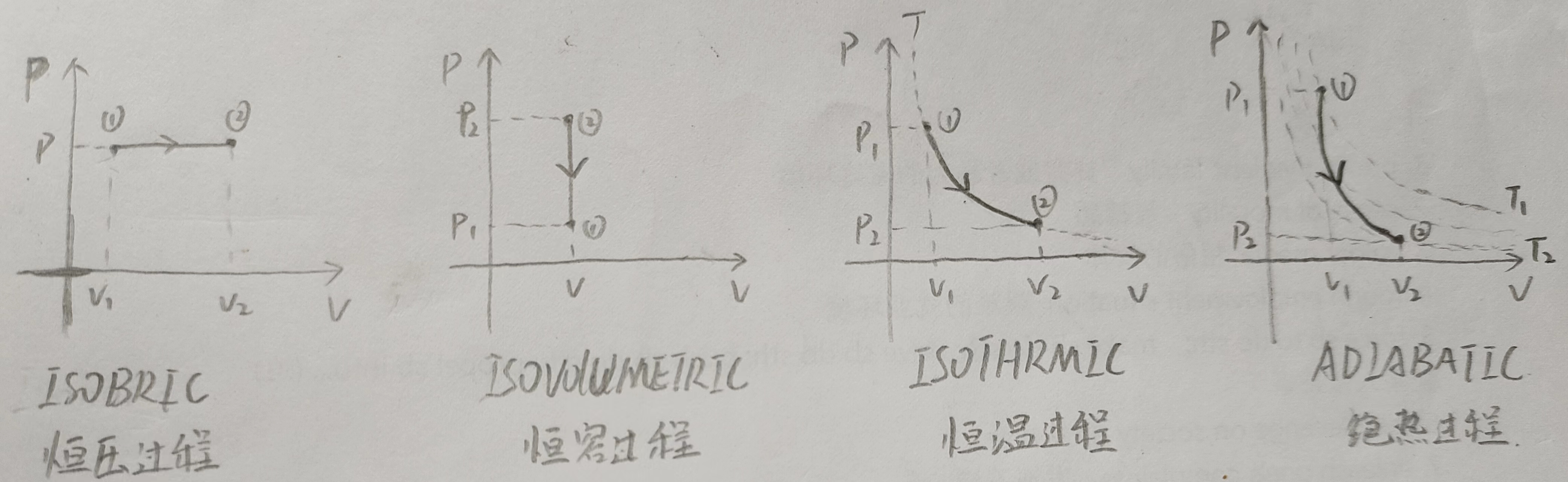
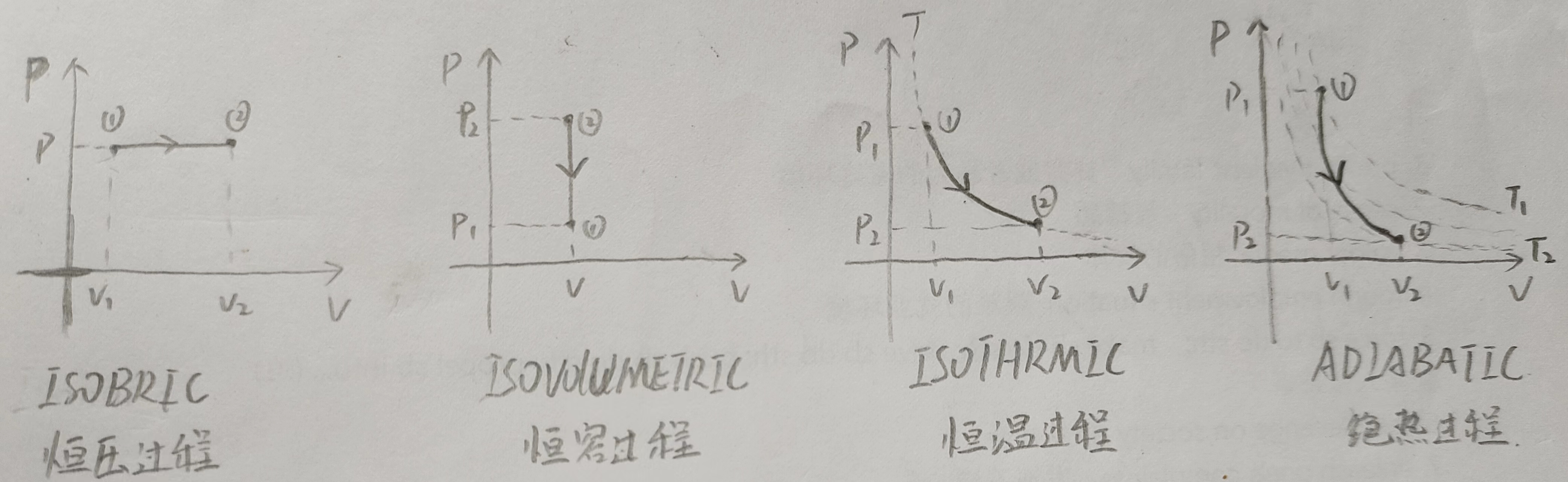
我们这里主要讨论上面四种PV图的\\(\\Delta U,Q,W\\), 其中\\(\\Delta U\\)是系统的内能,\\(Q\\)是系统吸收的能量,\\(W\\)是外界对系统做的功,我们在理想单原子气体上面讨论。
Preliminaries
我们一般把内能\\(U\\)看做温度和体积的函数,即\\(U= U(V,T)\\), 所以\\(U\\)的关于\\(V,T\\)的变化可以写为关于这二者的全微分
\\(dU = (\\frac\\partial U\\partial T)_VdT+(\\frac\\partial U\\partial V)_TdV\\)
又因为热一告诉我们
气体变化的内能等于气体吸收的热量与外界对其做功的和,即
\\(\\Delta U = \\Delta Q+\\Delta W\\)
对于一个可逆过程,有\\(\\Delta W = Fdx = -\\fracFAAdx = -pdV\\)(负号的意思是dv为负,体积减小,外界做正功), 这样有
\\(\\fracdQdT = \\fracdU+dWdT= (\\frac\\partial U\\partial T)_V+((\\frac\\partial U\\partial V)_T+p)\\fracdVdT\\)
对于恒容过程来说\\(dV = 0\\), 且因为第一项是在容器体积一定的情况下讨论的,所以有
$(\\fracdQdT)_V= C_V = (\\frac\\partial U\\partial T)_V $
即为恒容热容. 同样地,对于恒压过程来说,
\\((\\fracdQdT)_P = C_P = (\\frac\\partial U\\partial T)_V+((\\frac\\partial U\\partial V)_T+p)(\\frac\\partial V\\partial T)_p\\)
即为恒压热容。
现在考虑1摩尔理想的单原子气体,理想的单原子气体的内能\\(U\\)全部是粒子的动能,根据能量均分定理,我们有
\\(U = \\frac32RT = \\frac32Nk_BT\\)
所以有
\\(C_V = (\\frac\\partial U\\partial T)_V = \\frac32Nk_B\\)
所以有\\(U = C_VT\\)
这里\\(U\\)与\\(V\\)无关,即对于理想气体
\\((\\frac\\partial U\\partial V)_T = 0\\)
因为是理想气体,所以根据\\(PV= Nk_BT\\), 有
\\(\\frac\\partial V\\partial T = \\fracNk_BP\\)
\\(C_P = C_V+Nk_B = \\frac52Nk_B\\)
对于恒压过程
\\(\\Delta W = -PdV\\)
这里\\(dV\\)是大于0的,所以气体对外做正功,导致气体的内能减小,即对于数值来说
\\(\\Delta U = \\Delta Q -W\\)
这里\\(\\Delta U = \\frac32Nk_B\\Delta T\\), 所以数值上
\\(\\Delta Q = \\Delta U + W\\)
恒压过程中,根据\\(PV = Nk_BT\\), 体积增大,温度升高,所以\\(\\Delta U\\)是大于0的,这意味着\\(\\Delta Q\\)也是大于0的,所以这个过程中,气体会从外界吸收热量。
对于恒容过程
\\(\\Delta W = 0\\)
因为这里没有体积的变化,气体只有通过改变体积来对外做功,所以没有体积的变化就没有做功。所以\\(\\Delta U = \\Delta Q =\\frac32V(P_2-P_1) = \\frac32Nk_B\\Delta T=C_V\\Delta T\\)(第一个等号无论是在数值还是在符号上都成立)。
上述恒容过程中,同样地,体积不变,压强减小,温度降低,\\(\\Delta U\\)是小于0的,所以\\(\\Delta Q\\)是小于0的,所以这个过程中,气体会向外界放出热量。
对于恒温过程
因为是在恒温条件下,所以\\(\\Delta T = 0\\), 所以有:\\(\\Delta U =0\\)
所以数值上有\\(\\Delta Q = \\Delta W\\)
而数值上
\\(\\Delta W = \\int_v_1^v_2 \\fracNk_BTVdV = Nk_BT\\ln(\\fracv_2v_1) = P_1V_1\\ln(\\fracv_2v_1) = P_2V_2\\ln(\\fracv_2v_1)\\)
上述恒温过程中,体积增大,气体对外做正功,外界对气体做负功,所以\\(\\Delta W\\)是小于0的,这意味着气体能量在减小,温度会降低,但这是个恒温过程,所以此时必须吸收热量来补偿,所以\\(\\Delta Q\\)是大于0的。所以这个过程中,气体会从外界吸收热量。
对于绝热过程
因为绝热了,所以有\\(\\Delta Q = 0\\)
所以数值上有\\(\\Delta U = \\Delta W = C_V\\Delta T\\)
上述绝热过程中,气体膨胀对外做正功,所以外界对气体做负功,这意味着\\(\\Delta W\\)是小于0的,此时没有外界的热量补充,温度会降低,所以\\(\\Delta U\\)也是小于0的,也就是说绝热过程中,气体的内能是在减少的。
zend框架2流程图
我正在尝试理解ZF2流程,但如果没有像ZF1那样的流程图,那就太难了:
http://tournasdimitrios1.files.wordpress.com/2011/05/zend-framework-sequence_flowchart.jpg http://otroblogmas.com/wp-content/uploads/2010/07/zend-framework-flow-diagram.png
或者我如何记录在我的应用程序中调度的自定义事件?
有一张备忘单可供选择:
German Version of ZF2 Cheat-Sheet(不再提供)English Version of ZF2 Cheat-Sheet(不再提供)- English Version of ZF2 Cheat-Sheet (Alternative Link)
请注意,这些受版权保护,您不得在任何地方使用或重新分发。您只能链接到它们。
以上是关于Thermodynamics---PV Diagram的主要内容,如果未能解决你的问题,请参考以下文章