肠道微生物群影响眼部健康
Posted 谷禾牛博
tags:
篇首语:本文由小常识网(cha138.com)小编为大家整理,主要介绍了肠道微生物群影响眼部健康相关的知识,希望对你有一定的参考价值。
谷禾健康

人类肠道微生物组是一个多样化的生态系统,我们已经知道,它在多个器官系统健康中发挥着重要作用,肠道微生态失调可能导致各种常见疾病,如糖尿病、神经精神疾病、癌症等。
新的研究表明,肠道微生物组的改变与眼部疾病相关。
- 两项研究发现,在抗生素和无菌模型中,实验性自身免疫性葡萄膜炎评分降低,这表明肠道微生物群促进葡萄膜炎模型的发病。
- 研究年龄相关黄斑变性(AMD)的小鼠模型,发现AMD表型与梭菌门增加和拟杆菌门减少有关。
- 糖尿病视网膜病变的小鼠模型也显示,与对照小鼠相比,肠道微生物组成发生了变化。
基于小鼠实验,已经开始对人类微生物组及其与眼部病理学的关系进行临床研究。
葡萄膜炎、年龄相关性黄斑变性、青光眼、干眼综合征和霰粒肿等病理学正在探索中,对微生物组的深入研究可能扩展这些疾病的治疗方案。
本文总结目前检查肠-眼轴的临床研究,尤其是改变微生物组来缓解眼部疾病的潜在治疗方法。
01
为什么眼部健康可能与肠道相关?
研究发现,10% 的炎症性肠病患者会出现眼部疾病(巩膜外层炎、葡萄膜炎、结膜炎等)。肠道和与之相对较远的眼睛之间有什么关联?我们从以下几个方面来看:
▼
免疫系统
视网膜是眼睛后部的一层,里面装满了神经细胞,可以捕获图像并将其发送到大脑。
在所有的眼组织中,从免疫的角度来看,视网膜被认为是一种特权组织。它有三层保护(内部的血液-视网膜屏障;外层血视网膜屏障;以及血水屏障),以及通过“抵抗”和“容忍”策略,来保护它免受来自内部和外部环境的伤害。
这些血液视网膜屏障的变化可能通过募集炎症细胞和随后的眼内炎症导致视网膜疾病的发展,例如葡萄膜炎。
此外,它还受到自身防御系统的保护,如小胶质细胞和补体系统,以维持视网膜稳态。
视网膜由于更新和修复能力差而非常脆弱,因此即使是轻微的损伤也会产生毁灭性的后果。
年龄相关性黄斑变性是一种全身免疫性疾病,局部表现为眼部免疫环境下调所致。免疫反应改变的迹象表现为先在视网膜色素上皮中逐渐积累,后在玻璃膜疣中逐渐积累的沉积物,构成有利于免疫系统显著激活的抗原刺激。
在衰老过程中,所有防御系统的效率都会降低,与年龄相关的形态功能和免疫变化伴随着慢性低水平炎症。“炎症”过程也会导致与年龄相关的视网膜疾病。
▼
肠道通透性
眼睛的物理变化被认为是由于肠道内壁的炎症与肠道通透性增加有关。肠道通透性/肠漏综合征的变化允许细菌、毒素或免疫化合物穿过粘膜肠道屏障并传播到不同位置,包括眼睛表面。这些化合物直接影响眼睛或可能通过分子模拟引发眼睛的免疫反应。分子模拟是一种可能引发自身免疫性炎症的机制,因为保护屏障受损以及细菌或毒素的长期存在。
扩展阅读:
什么是肠漏综合征,它如何影响健康?
▼
肠道微生物群及其代谢产物
在许多层面上,肠道微生物群和免疫化合物与眼睛的视网膜相互作用。不健康、失调的肠道微生物群和活化的免疫细胞会在眼睛中引发炎症,并影响视网膜、眼睛微生物组和眼睛润滑,从而导致眼部相关疾病。
肠道微生物组及其代谢物,尤其是短链脂肪酸,都可以通过直接或间接修改不同细胞类型的表观基因组来调节免疫细胞的关键功能。
损害眼睛的危及视力的免疫反应是眼内炎症性疾病的典型特征。葡萄膜炎、年龄相关性黄斑变性、与干眼症相关的干燥综合征、糖尿病视网膜病变、青光眼和感染性角膜炎与肠道微生物组异常有关。
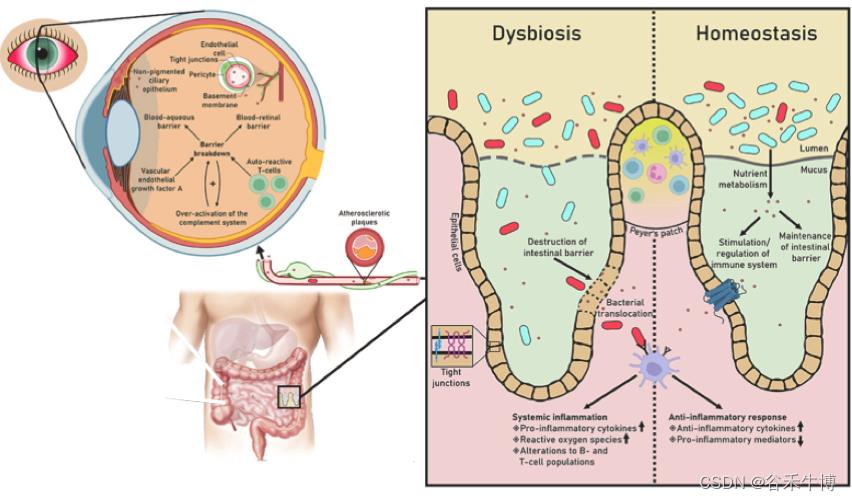
doi.org/10.1016/j.preteyeres.2022.101117
接下来,我们来看一下具体哪些肠道菌群与眼部相关疾病有关。
02
与眼部疾病状态相关的菌群变化
▼
糖尿病视网膜病变
在糖尿病视网膜病变中,与健康对照组相比,主要的分类门,包括拟杆菌门、放线菌门、粪杆菌门和梭菌门被耗尽。
在两项评估糖尿病视网膜病变队列中微生物组多样性的研究中,发现多样性下降,这与临床前小鼠模型一致。
▼
色素性视网膜炎
与对照小鼠相比,Bacteroides caecimuris在患病小鼠中显着增高。受影响的小鼠缺少健康肠道微生物组典型的菌群,如Rikenella,Muribaculaceae, Prevotellaceae UCG-001, Bacilli 等。
肠道微生物组变化与眼部疾病之间的联系可以通过多种机制来解释。肠道生态失调可以有利于增加肠道通透性,允许微生物及其代谢物诱导眼细胞炎症。微生物失衡也可能是血液视网膜屏障破裂和中枢神经系统氧化应激增加的原因。所有这些假设也可以解释视网膜色素变性小鼠模型中的神经炎症,氧化应激和细胞死亡。
▼
年龄相关性黄斑变性
年龄相关性黄斑变性( ARMD )是一种多因素疾病,由遗传和环境因素的复杂组合引起。
与改变的肠道微生物群相关的肠道通透性增加,允许肠道代谢物和产物的更高易位,可能调节视网膜特异性免疫细胞。有趣的是,LPS 引起的慢性炎症会加速营养不良 P23H 大鼠的神经变性,导致营养不良视网膜的形态和生理紊乱恶化。
宏基因组测序评估了 ARMD 患者和对照组,研究人员发现 ARMD 患者中以下菌群含量较高 :
- Anaerotruncus
- Oscillibacter
- Ruminococcus torques
- Eubacterium ventriosum
而以下菌群在对照组中含量较高:
- Bacteroides eggerthii
研究人员推测可能与谷氨酸降解和精氨酸生物合成途径增加有关。谷氨酸是一种众所周知的视网膜兴奋性神经递质,因此其减少可能导致视网膜神经传递不足。
关于谷氨酸代谢详见:兴奋神经递质——谷氨酸与大脑健康
此外,患者也缺乏负责脂肪酸延伸途径的细菌。在这方面,长链多不饱和脂肪酸可能对视网膜生理学产生关键影响,并可能促进ARMD发展。
相比之下,对照组中Bacteroides eggerthii 的丰度可能对该疾病具有保护作用,因为它能够产生短链脂肪酸。这些代谢产物可能通过改变淋巴细胞从肠道向眼睛的迁移来调节眼内炎症。
▼
新生血管性年龄相关性黄斑变性
一项针对12名新生血管性年龄相关性黄斑变性(nAMD)患者的试验发现,与对照组相比,nAMD患者存在“微生态失调”。值得注意的是,研究人员发现了Anaerotruncus的增加,这也与小鼠模型中炎症信号的增加有关,这表明肠道微生物变化和nAMD进展相关的可能作用机制。
▼
青光眼
在青光眼患者中,研究人员发现肠易激综合征是一种与微生物群失调相关的疾病,会显著增加患青光眼的几率(OR=5.84)。
除了发现青光眼患者与对照组的细菌谱存在差异外,还注意到视觉效果与巨单胞菌和Blautia属的丰度呈负相关。
扩展阅读:
肠道核心菌属——巨单胞菌属(Megamonas),不同人群差异大
肠道核心菌属——经黏液真杆菌属(Blautia),炎症肥胖相关的潜力菌
▼
特发性颅内高压
一项视网膜研究了一组特发性颅内高压患者,再次发现与对照组相比微生物群存在差异。
有趣的是,使用乙酰唑胺治疗的患者发现乳酸杆菌增加,这被认为对肠道微生物健康有益。
总的来说,在眼部病理中,菌群可能发生改变或破坏,见下表:
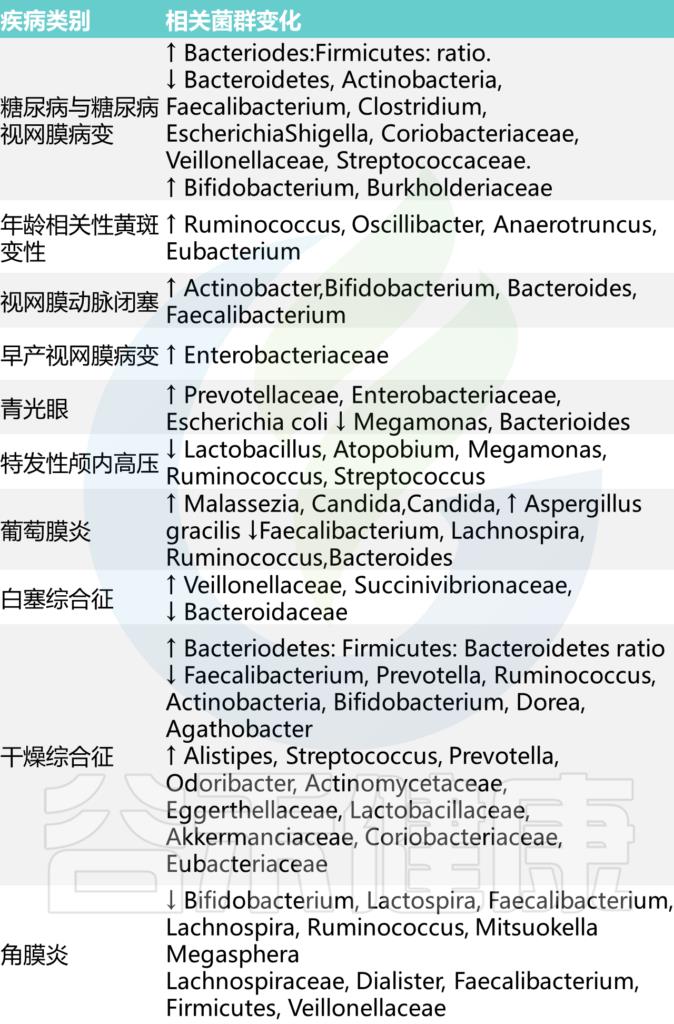
Russell MW, et al., Eye (Lond). 2023
03
影响眼部健康的肠道微生物群及其代谢产物
肠道微生物组可以调节炎症信号的变化。因此,如果肠道组织受到影响,导致全身促炎状态,那么眼部后果可能是继发于或平行于肠道炎症轴的,或者可能在主要过程中有所不同。
▼
真菌也可能参与角膜炎等眼部疾病
在葡萄膜炎的情况下检查了肠道失调,发现各种抗炎微生物群减少。但也有研究人员注意到葡萄膜炎的肠道失调,病例和对照组之间的没有显著差异,研究人员认为细菌可能与这种病理状态无关。
进一步探讨这种可能性,有研究人员发现,与对照患者相比,致病性念珠菌属和曲霉菌属增加了。另一项研究发现与对照患者相比,角膜炎患者的肠道失调,这两项研究都发现了标记的细菌群落变化。这些研究也检测了真菌的变化,注意到致病性曲霉、念珠菌和马拉色菌增加的趋势,这些真菌已被证明表现出抗真菌耐药性并参与其他疾病过程。
两项试验检测了白塞病葡萄膜炎患者的微生物群差异,发现病例和对照组之间存在显著差异。白塞病患者的微生物群多样性也显著降低。上述数据表明肠道健康和眼部病理之间可能存在联系。
然而,目前尚不清楚真菌和细菌是否直接介导眼部病理,是否与免疫系统有关,或者是否有其他未发现的途径在起作用。
扩展阅读:膳食真菌在癌症免疫治疗中的作用: 从肠道微生物群的角度
▼
菌群代谢产物TMAO可能也在眼病中发挥作用
研究人员发现,视网膜动脉阻塞(RAO)患者与健康对照相比,不同分类属的细菌有所增加。这项研究还发现RAO患者的三甲胺-N-氧化物(TMAO)显著增加,TMAO是一种微生物群衍生的代谢产物,已被发现是心血管不良事件、死亡率和血栓形成的独立风险因素。
在这项研究中,TMAO和阿克曼菌Akkermansia丰度呈正相关,表明微生物群和RAO之间存在潜在的机制联系。然而,必须注意的是,在其他研究中,Akkermansia被发现与TMAO浓度呈负相关,这表明TMAO可能不是病因,或者,TMAO本身可以在眼部病理学中发挥中介或主要作用。如上所述,这项研究并不是为了证明一种联系,也不是为了简单地假设一种联系的存在。
肠道微生态失调的眼部临床研究
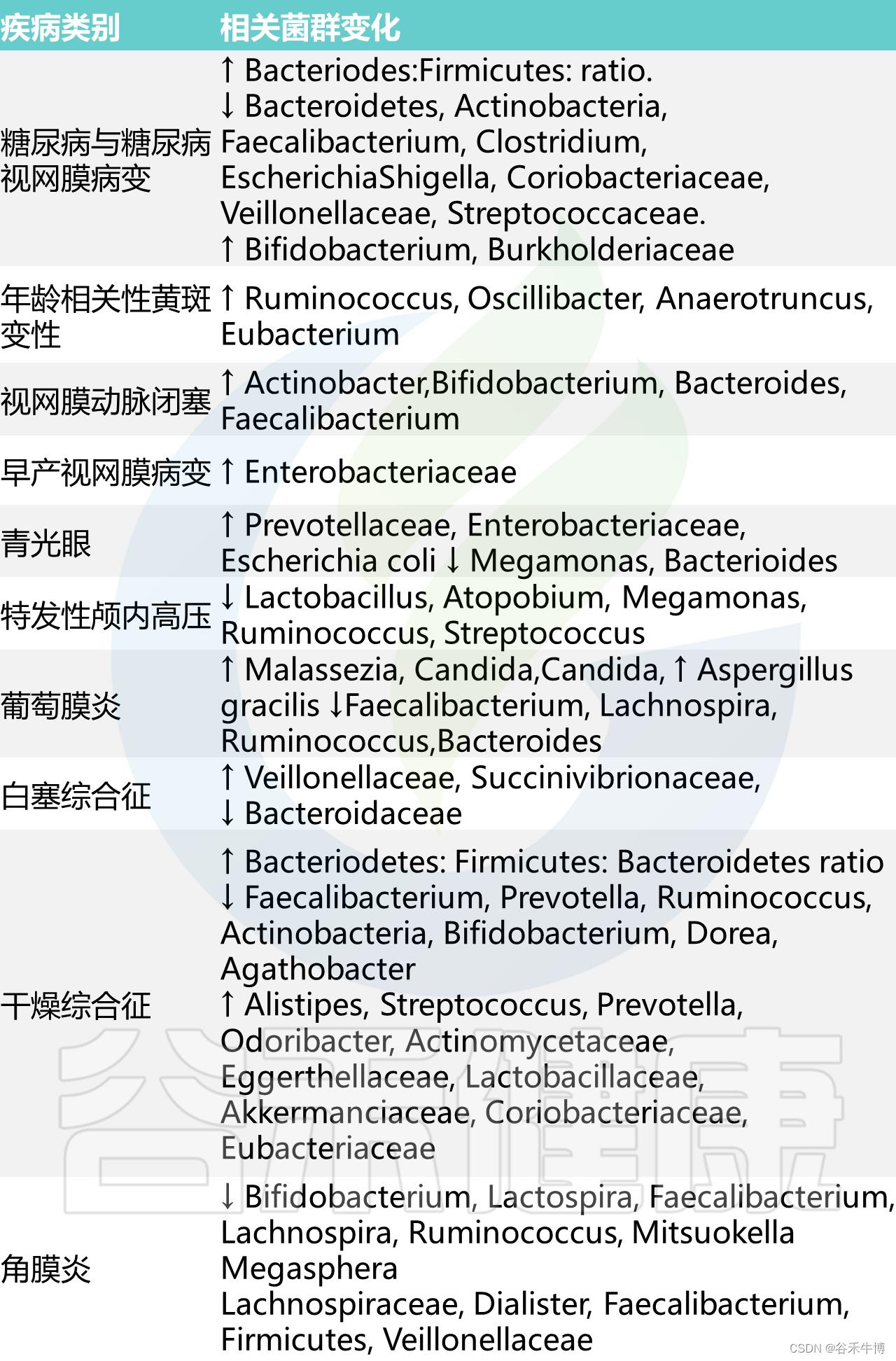


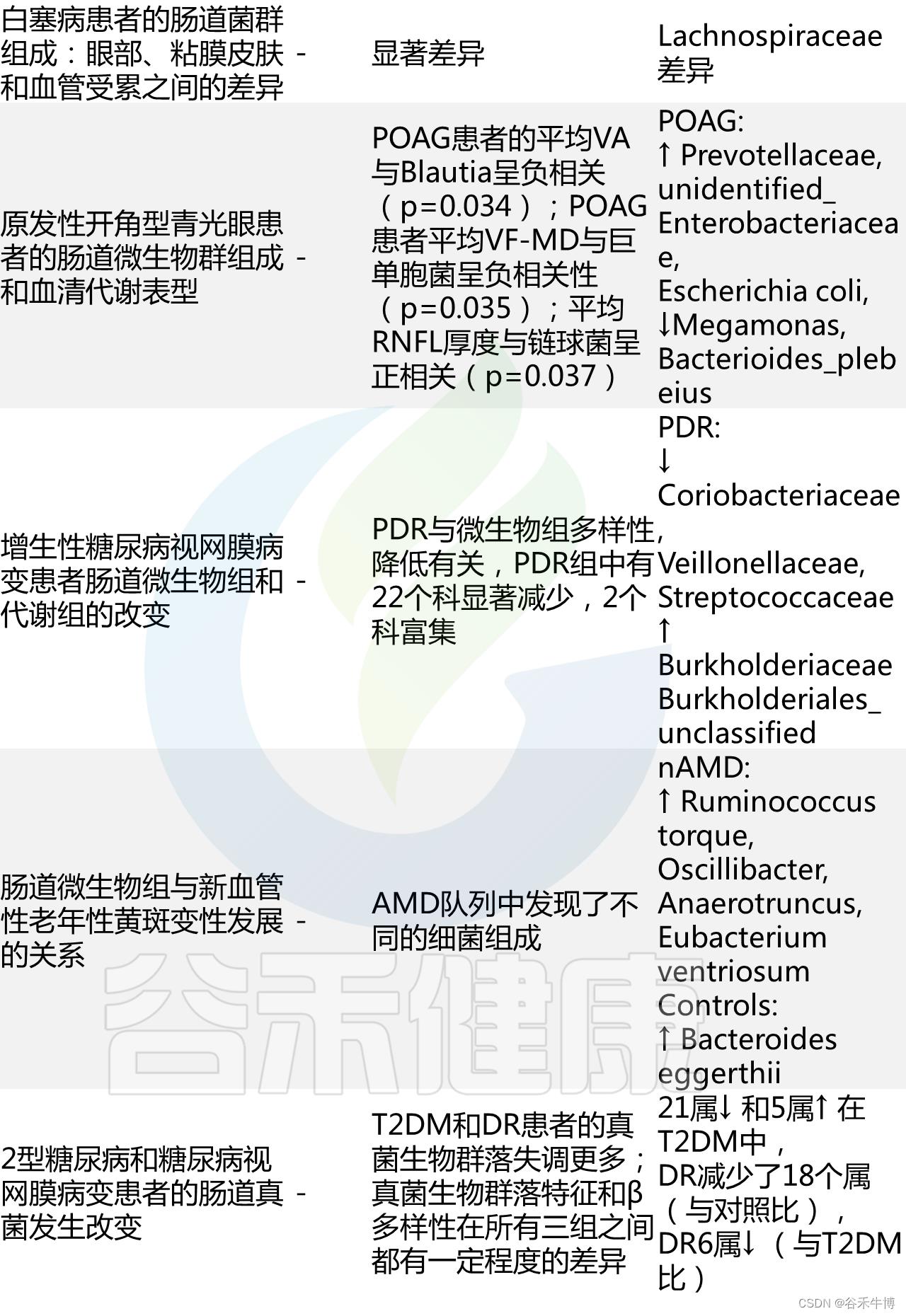
Russell MW, et al., Eye (Lond). 2023
04
基于微生物群改善眼部疾病的方法(临床研究)
有四项临床研究(≤23名患者)通过粪菌移植(FMT)或益生菌补充靶向肠道微生物群,来治疗眼部疾病。
▼
粪菌移植
Watane等人于2021年对10例干燥综合征并发干眼症的患者进行了粪菌移植。粪菌移植后三个月,没有副作用报告,患者自我报告的干眼症症状在一半的队列中减轻了。
▼
益生菌补充剂
Filippelli等人于2021和2022年对10名成人和13名儿童患者的益生菌补充剂及其治疗霰粒肿的疗效进行了研究。在这两项研究中,均使用了含有嗜热链球菌、乳酸乳球菌和德氏乳杆菌的益生菌。所有接受益生菌制剂治疗的成年患者霰粒肿消退时间显著缩短,而这种影响对于只有小于2.0mm的小霰粒肿的儿童来说也是如此。
Napolitano等人于2021报道了一例有三年前葡萄膜炎病史的患者的病例。患者服用了含有乳酸双歧杆菌、两歧双歧杆菌和短双歧杆菌的益生菌补充剂。两个月后,该患者的视觉功能增加,葡萄膜炎的临床症状减少。益生菌配方并不包括患者微生物组中不存在的物种。
扩展阅读:如果你要补充益生菌 ——益生菌补充、个体化、定植指南
除了以上的临床研究外,其他可能的干预措施:
▼
高纤维饮食
高纤维饮食会促进某些细菌在肠道中占据优势地位,这些细菌会产生短链脂肪酸,促进调节性 T 细胞分化,并降低发生眼部炎症的倾向。一些实验正在直接使用短链脂肪酸来测试它作为肠外自身免疫性疾病的治疗干预,已有研究人员发现,在小鼠身上,它对自身免疫性葡萄膜炎有保护作用。
▼
避免高血糖饮食
一项涉及衰老小鼠的研究中,高血糖饮食导致光感受器退化和视网膜色素上皮细胞萎缩,这在喂食正常饮食的小鼠中是看不到的。恢复到低血糖饮食可以逆转疾病的特征,并改变肠道中 AMD 保护因子(包括血清素)的水平。
▼
避免高脂饮食
高脂饮食会导致肠道渗透性增加,从而使细菌产物如脂多糖和其他病原体相关分子模式的分子易位增加,它们通过先天免疫系统的模式识别受体 ( 特别是Toll样受体和Nod样受体)影响促炎信号转导,引起低度全身性炎症,加剧脉络膜新生血管形成,最终加重病理性血管生成。
在一项研究中,在4周龄的C57BL/6小鼠中研究了高脂肪饮食对泪腺功能的影响。结果显示,高脂饮食的小鼠表现出病理变化,包括眼泪分泌水平降低、炎症性CD4+T细胞增加 ,细胞浸润、TNF-α和IL-1β等促炎因子增加以及腺泡和肌上皮细胞凋亡增加。将标准饮食引入之前高脂肪饮食的小鼠后,泪腺的病理变化部分逆转,包括炎症细胞和促炎因子的减少以及抗炎胞质分裂素的上调。
▼
间歇性禁食
在啮齿动物模型中,在开始隔日禁食方案后的 1 周内,间歇性禁食已被证明可以降低血压和心率,这两者都是 糖尿病性视网膜病变等眼部血管疾病的已知危险因素。
另一项早期限时喂养(从早上 8 点到下午 2 点随意喂养,剩下的 18 小时禁食)被证明可以降低餐后胰岛素、血压、氧化应激和夜间食欲同时增加人类受试者的胰岛素敏感性和 β 细胞功能。这项研究和其他研究进一步支持间歇性禁食的有益作用,并表明它可能通过降低血压和胰岛素敏感性来治疗眼部血管疾病。
连续 7 个月的隔日禁食,增加了产生肠粘液的杯状细胞的数量,并降低了血浆 PGN 的浓度,表明肠血管屏障完整性得到改善。
- 间歇性禁食显示通过增加 F/B 比来改善肠道微生物群。
- 间歇性禁食通过增加有益次级代谢物(例如牛磺熊去氧胆酸盐 TUDCA)的产生来改变胆汁酸代谢。
- 间歇性禁食通过减少小鼠中视网膜脱细胞毛细血管的数量来改善糖尿病性视网膜病变病理学。
扩展阅读:间歇性禁食 & 肠道菌群 & 心血管代谢疾病
▼
补充剂——锌
动物研究表明,锌通过减少氧化应激来改善视网膜的抗氧化过程。特别是,肠道菌群竞争锌的供应,锌对共生代谢途径和细菌毒力因子都很有用。然而,锌缺乏及其过量的存在都会改变微生物组的组成。
扩展阅读:膳食锌缺乏或过量对人体肠道菌群及健康的影响
▼
类胡萝卜素、叶黄素
膳食补充类胡萝卜素和锌可以预防或延缓眼部疾病的进展,可能是通过它们的抗氧化和抗炎特性。叶黄素和玉米黄质两种叶黄素,它们天然集中在人眼的黄斑中。它们充当蓝光的光学滤光片,并作为常驻抗氧化剂和自由基清除剂,以减少氧化应激引起的损伤。
由于人类无法合成类胡萝卜素,因此供应取决于含类胡萝卜素的食物,例如绿叶蔬菜、西兰花、豌豆、玉米和蛋黄。
▼
omega-3 长链多不饱和脂肪酸 (LCPUFA)
大量摄入 omega-3 长链多不饱和脂肪酸 (LCPUFA) 与年龄相关黄斑变性风险降低有关。而大量摄入 omega-6 LCPUFA 与风险增加有关。LCPUFAs高度集中在眼睛中,对视网膜的视觉功能至关重要。此外,它们是对氧化应激的促炎和抗炎免疫反应的重要调节剂。ω-3和ω-6 LCPUF之间的比例似乎对预防慢性低度炎症很重要。可以通过某些富含脂肪的鱼,亚麻籽和藻类等补充。
▼
膳食多酚
膳食多酚可减少氧化应激,在视网膜色素上皮细胞中具有抗炎作用,并与各种白细胞介素和信号通路的调节有关。在丁香、浆果、红酒或绿茶中富含。
扩展阅读:肠道微生物群与膳食多酚互作对人体健康的影响
其他对眼部健康至关重要的营养物质包括:
维生素 A、番茄红素、硫辛酸、维生素 C、姜黄素、白藜芦醇、槲皮素、葡萄籽提取物、绿茶提取物等。
05
微生物群与眼部疾病研究方向和挑战
微生物组的复杂性对研究微生物变化有挑战,因为微生态失调可能归因于多种菌群的同时过度生长或损失。目前的文献并没有直接分析出因果关系。
除了目前的试验涉及的非特异性干预之外,其他干预措施也可能有效果。一项对36名患者进行的17周的随机前瞻性研究表明,通过逐步引入发酵食品等相对不那么激烈的措施,可以对免疫功能产生类似的影响。
关于发酵食品详见:肠道微生物群与健康:探究发酵食品、饮食方式、益生菌和后生元的影响
也有研究人员认为,应该谨慎采用通过改变微生物组来改善系统健康的干预措施。30名患者使用益生菌增加微生物多样性,然而却因这种补充而患上了小肠细菌过度生长和D-乳酸酸中毒。开始抗生素治疗后,患者症状减轻(P=0.005)。
由于许多原因,选择与疾病相关的正确益生菌并不容易。同一属和种的不同菌株可能对宿主产生完全不同的影响。应充分了解特定细菌菌株的特定特性和特征以及对宿主健康的影响。
因此,需要更大规模的前瞻性临床试验研究益生菌补充剂对各种眼部疾病的影响,对于进一步阐明这些干预措施的疗效至关重要。有必要研究在剂量和配方方面选择更合适的益生菌方案。
为了建立肠道菌群与眼部病变缓解之间的因果治疗关系,未来的研究可能考虑将微生物组-免疫-眼部效应与纯粹的微生物组-眼部效应分离开来。
结 语
临床试验检查了肠道微生物群和眼部病理之间的联系,显示了这两个系统之间的联系。
通过饮食、益生元和益生菌以及粪菌移植等方式调节肠道微生物群,可能都会成为预防和/或治疗眼部疾病的有效方案。
充分结合肠道菌群检测全面评估患者的菌群健康状况,可以考虑采用更有针对性的干预措施,而不仅仅是粪菌移植和益生菌补充剂。
大规模的随机对照临床试验可能会进一步证明这种联系,并阐明新的靶点治疗机制。
主要参考文献:
Zysset-Burri DC, Morandi S, Herzog EL, Berger LE, Zinkernagel MS. The role of the gut microbiome in eye diseases. Prog Retin Eye Res. 2023 Jan;92:101117. doi: 10.1016/j.preteyeres.2022.101117. Epub 2022 Sep 6. PMID: 36075807.
Napolitano P, Filippelli M, Davinelli S, Bartollino S, dell'Omo R, Costagliola C. Influence of gut microbiota on eye diseases: an overview. Ann Med. 2021 Dec;53(1):750-761. doi: 10.1080/07853890.2021.1925150. PMID: 34042554; PMCID: PMC8168766.
Russell MW, Muste JC, Kuo BL, Wu AK, Singh RP. Clinical trials targeting the gut-microbiome to effect ocular health: a systematic review. Eye (Lond). 2023 Mar 14. doi: 10.1038/s41433-023-02462-7. Epub ahead of print. PMID: 36918627.
Shivaji S. A systematic review of gut microbiome and ocular inflammatory diseases: Are they associated? Indian J Ophthalmol. 2021 Mar;69(3):535-542. doi: 10.4103/ijo.IJO_1362_20. PMID: 33595467; PMCID: PMC7942081.
Bai X, Xu Q, Zhang W, Wang C. The Gut-Eye Axis: Correlation Between the Gut Microbiota and Autoimmune Dry Eye in Individuals With Sjögren Syndrome. Eye Contact Lens. 2023 Jan 1;49(1):1-7. doi: 10.1097/ICL.0000000000000953. Epub 2022 Nov 11. PMID: 36544282.
Scuderi G, Troiani E, Minnella AM. Gut Microbiome in Retina Health: The Crucial Role of the Gut-Retina Axis. Front Microbiol. 2022 Jan 14;12:726792. doi: 10.3389/fmicb.2021.726792. PMID: 35095780; PMCID: PMC8795667.
当营养遇上肠道菌群:探究其对儿童健康的影响
谷禾健康

越来越多的证据表明,肠道菌群定植紊乱和微生物多样性减少与全球非传染性疾病 (NCD) 的增加有关。影响儿童和青少年的非传染性疾病包括肥胖及其相关合并症、自身免疫性疾病、过敏性疾病和哮喘。饮食变化也与非传染性疾病的发病机制有关,并且由于饮食是肠道微生物群组成和功能的主要驱动因素之一,因此人们开始关注通过饮食干预,来促进健康的肠道微生物群,最终促进健康。
一些生物活性营养素,如长链多不饱和脂肪酸 (LC-PUFA)、铁、维生素、蛋白质或碳水化合物,已被确定在婴儿出生后的前 1000 天对婴儿生长、神经发育发挥重要作用,以及肠道菌群的建立和成熟。LC-PUFA 是中枢神经系统 (CNS) 的结构成分,对视网膜发育或海马可塑性至关重要。最近,乳脂球膜 (MFG) 的成分被添加到婴儿配方奶粉中,因为它们在婴儿发育中起着关键作用。
大量摄入蛋白质会导致婴儿期体重增加更快,但这与后来的肥胖有关。可消化的碳水化合物提供葡萄糖,这对中枢神经系统的充分运作至关重要;不易消化的碳水化合物 [例如人乳低聚糖 (HMO)] 是肠道细菌的主要碳源。婴儿期缺铁性贫血与精神和精神运动发育的改变有关。与维生素 B6 和 B12 密切相关的叶酸代谢控制表观遗传变化。
从历史上看,重点一直放在早期营养对生长模式和儿童体脂成分的影响上。证据表明,生命早期摄入过多的能量和快速或缓慢的生长模式与不良的发育结果有关;事实上,婴儿期体重快速增加是晚年肥胖的重要预测指标。
肠道菌群与营养失调与多种儿科疾病有关,营养素的摄入和肠道微生物群的定植和成熟是相互关联的,因此通过饮食干预来促进健康的肠道微生物群是一种有前途的方法,可以改善儿童健康结果。

本文讨论和总结评估营养和肠道微生物群对儿童健康结果影响的临床研究的最新发现,并分享使用营养方法有利地改变肠道微生物群以改善儿童健康结果的研究成果。
01
生命第一年的重要营养素与肠道微生物
★ 脂 肪
脂肪酸是许多脂质的主要成分,必须通过婴儿饮食提供必需的脂肪酸,以实现健康成长、神经发育、免疫系统和胃肠功能。
婴儿的脂肪摄入量占比
在生命的头几个月,多不饱和脂肪酸 (PUFAs) 的需求增加,因为快速生长和神经发育。婴儿的脂肪摄入量在母乳喂养期间很高,从开始添加辅食后的第一年下半年逐渐减少。脂肪营养需求量占每日总能量摄入:
- 0 ~ 6 个月是 50-55%
- 6 ~ 12 个月是 30-40%
- 12 ~ 36 个月是 35-40%
细分各类脂肪酸的摄入量
最近,不同的国家确定亚油酸的摄入量应占总能量的 4%,而 α 亚麻酸应占总能量的 0.5%。
长链多不饱和脂肪酸 (LC-PUFAs)、n-3 二十二碳六烯酸 (DHA, 22 : 6n-3) 和花生四烯酸 (ARA, 20 : 4n-6) 是中枢神经系统细胞膜的功能成分,在神经传递具有关键作用。
欧洲食品安全局 (EFSA) 委员会已确定:
0 ~ 24 个月的 DHA 摄入量为 100 毫克/天;
0 ~不到6个月的 ARA 摄入量为 140 毫克/天;
ARA 和 DHA 由母乳提供
婴儿的 DHA 状态是通过母乳提供的,它取决于母亲的 DHA 状态;尽管如此,母乳中的 ARA 浓度始终接近总脂肪酸的 0.5%,通常高于 DHA,与 DHA 相比更稳定。
与大脑发育相关的脂肪酸
大量的 n-3 和 n-6 LC-PUFA 在器官和组织的膜中迅速积累。在胎儿生命的最后三个月和生命的头两年,DHA 在脑组织中积累,特别是在与注意力、运动控制和感觉统合相关的灰质区域,而 ARA 负责海马可塑性。
已经表明,ARA 的延伸产物肾上腺酸 (ADA,22:4n-6) 是细胞膜中的重要成分。ADA构成了大脑中近一半的n-6 LC-PUFA,n-6 LC-PUFA的含量远远超过n-3 LC-PUFA。
均衡摄入DHA和ARA对大脑功能和发育至关重要
事实上,生命早期较高的 DHA/ARA 比率与更好的认知结果相关。已经表明,神经发育结果有利于 DHA 与 ARA 的比例为 1:1 或 1:2,而与1:1和1:2的比例相比,1.5∶1的比例会降低大脑发育过程中红细胞中ARA的浓度。
在脂肪酸摄入量和线性生长之间建立关系的研究得出了不同的结论。其中一些人认为必需脂肪酸对于婴儿期的最佳线性生长很重要,也有研究人员没有发现任何关联。
乳脂球膜蛋白的健康益处
另一方面,脂肪的研究工作表明,乳脂球膜 (MFGM) 蛋白代表母乳的生物活性部分,可提供一些健康益处。这种膜组分由不同的生物活性成分(磷脂酰胆碱、鞘磷脂、胆固醇和脑苷脂、神经节苷脂等)组成,它们对大脑发育和免疫功能有积极影响并保护新生儿胃肠道调节肠道菌群组成。
饮食中脂肪酸的分布与肠道菌群的关联
我们通常认为饮食中脂肪过多会造成肥胖,实际上,饮食中脂肪酸的分布也可能改变肠道微生物群的组成和肥胖状况。最近,表明人乳中的 sn-2 脂肪酸与婴儿肠道微生物群之间存在显着关联;ARA 和 DHA 与拟杆菌属(Bacteroides)、肠杆菌科(Enterobacteriaceae)、韦荣球菌属(Veillonella)、链球菌属(Streptococcus)和梭菌属(Clostridium)有关,参与短链脂肪酸(乙酸盐、丙酸盐和丁酸盐)生产的细菌,具有重要的免疫调节功能,在抵抗肠道病变的发展等方面发挥着关键作用,并且在母乳喂养后 13-15 天显着增加。
扩展阅读:脂肪毒性的新兴调节剂——肠道微生物组
如何通过喂养菌群产生丁酸调节人体健康
★ 蛋白质
蛋白质在生命的前 1000 天非常重要,因为它们在细胞结构中发挥着重要作用,并且是酶和神经递质的组成部分。
蛋白质推荐量
在出生后的头 6 个月内,每公斤体重/天的蛋白质推荐量为:
0 至 6 个月大时为 0.58 克;
6 至 36 个月大时为 0.66 克。
母乳中蛋白质种类多,有多种功能
母乳含有 400 多种蛋白质,多种功能如抗菌、免疫调节活性或刺激营养吸收等。蛋白质缺乏会导致生长发育不良以及运动和认知发育迟缓;然而,高蛋白质摄入会导致婴儿期体重增加更快,并与以后的肥胖相关。
使用婴儿配方奶粉喂养的婴儿在生命的前四个月内表现出正常的婴儿生长模式,婴儿的总蛋白质减少 1.0 g/dl(类似于母乳)。
辅食中蛋白质影响婴儿生长及肠道菌群组成
补充食品中的蛋白质来源和摄入量会显着影响婴儿生长并可能影响超重风险;以肉类和奶制品为基础的辅食会导致不同的生长模式,尤其是身高。
同时,补充喂养期间相关类型的富含蛋白质的食物,对配方奶喂养婴儿的肠道微生物组成和代谢物有影响;吃肉的儿童肠道群落富含厚壁菌门和粪杆菌属,同时变形杆菌门和双歧杆菌属减少。
扩展阅读:肠道菌群与蛋白质代谢
认识变形菌门,变形菌门扩张的原因和健康风险
★ 碳水化合物和糖
碳水化合物需求量
每日总能量摄入中的总碳水化合物需求量占比如下:
0 ~ 6 个月为 40-45%
6 至 12 个月以下为 45-55%
12 至 36 个月以下为 45-60%(接近成年人)
葡萄糖
葡萄糖对于中枢神经系统的充分运作起着关键作用,因为它是生长、神经冲动和突触的主要能量来源。葡萄糖由不同的碳水化合物提供给婴儿,例如乳糖,作为母乳中的主要糖分(范围为 6.7 至 7.8 g/dl),以及多种低聚糖,其含量约为 1 g/dl。
母乳低聚糖
母乳低聚糖 (HMO) 构成了婴儿无法消化的母乳碳水化合物的重要部分。母乳低聚糖具有益生元功能,可喂养胃肠道微生物群,并促进有益菌的生长;此外,它们还与多种生物学功能有关,例如对胃肠道发育和全身免疫的影响、双歧杆菌生成活性和抗感染、炎症调节、肠神经元激活和肠道运动,以及中枢神经系统功能的增强。
母乳低聚糖包括酸性低聚糖,主要是唾液酸化 [例如 6'-唾液酸乳糖 (6'-SL)、3'-唾液酸乳糖 (3'-SL)] 或中性低聚糖 [例如 2'-岩藻糖基乳糖 (2'-FL)]。
岩藻糖基聚糖是母乳中最丰富的母乳低聚糖形式 (80–90%) 。
聚糖
聚糖(glycans)是微生物的碳源,对宿主细胞和微生物之间的识别、信号传导和表观遗传调控至关重要,与广泛的免疫和代谢紊乱有关。双歧杆菌属和乳杆菌属与的生长之间存在显着相关性。在哺乳早期和晚期的婴儿肠道中。
几个临床前模型已经证明母乳低聚糖对认知功能的影响,但人类的临床数据尚未公布。
关于糖没有特定推荐量,2岁以下避免添加糖
关于糖,没有针对婴儿期糖的特定的每日参考摄入量。ESPGHAN 营养委员会建议,避免在 2 岁以下儿童的饮食中添加糖分。还建议避免饮用果汁或含糖饮料,因为过早摄入这些饮料会增加日后患 1 型糖尿病的风险。
★ 铁
为什么婴儿在 6 个月左右时需要添加辅食?与铁等营养素的需求有关
在婴儿出生前,胎儿会从母体中吸收铁元素,积累在肝脏中,以备出生后使用。然而,母乳中的铁含量相对较低,因此在婴儿 6 个月左右时,需要从饮食中摄取外源性铁以满足营养需求。
铁的需求量
0 ~ 6 个月为 0.3 毫克/天;
6 ~ 12 个月以下为 6-11 毫克/天;
12 ~ 36 个月以下的需求量为 3.9-9 毫克/天。
缺铁有哪些影响?
缺铁会影响大脑、神经和精神运动发育,因为铁是神经递质所需酶的组成部分。缺铁会导致携氧能力降低,从而导致生长发育所需的葡萄糖转化受限;这些限制可能导致生长迟缓、体重减轻和年龄增长,但与神经发育不同的是,它们可以通过补铁治疗来克服。
缺铁影响肠道菌群组成
母乳是短双歧杆菌的主要来源,它可以在二价金属通透酶和乳铁蛋白的帮助下获得管腔铁,促进这些有益细菌的生长,并从细菌病原体中隔离铁。缺铁导致肠道微生物群落失调,这反映在肠杆菌科(Enterobacteriaceae)和韦荣球菌科(Veillonellaceae)的相对丰度增加,以及与健康对照相比,红蝽菌科(Coriobacteriaceae)肠杆菌科和双歧杆菌科/肠杆菌科的丰度降低。
Coriobacteriaceae被确定为一个潜在的生物标志物,将运动与健康改善联系起来。
扩展阅读:人与菌对铁的竞争吸收 | 塑造并控制肠道潜在病原菌的生长
★ 维生素 D
纯母乳喂养的婴儿摄入的维生素 D 低于最低推荐摄入量,远低于每日参考摄入量。
维生素D推荐摄入量
为避免因维生素D而可能出现的病症,例如骨矿化不足或软骨病,母亲每天补充 400 至 2000 IU 可以增加母乳中的维生素 D 水平;建议纯母乳喂养的婴儿接受阳光照射和补充维生素 D。
0 至 36 个月以下的婴儿维生素 D 营养需求为:
10 微克/天。
缺乏维生素D会引起什么?
维生素D诱导神经生长因子,促进神经突生长,抑制海马神经元凋亡。关键神经发育时期的缺陷会导致生命后期的行为、记忆和学习障碍。
低水平的维生素 D 会导致肠道通透性增加,产生慢性低度炎症状态。
维生素 D 与肠道菌群之间存在关联,在 3-6 个月大的不同种族婴儿的肠道微生物群组成中观察到一些差异,这些婴儿的母亲在怀孕期间补充了维生素 D 以预防其后代的哮喘和过敏症。
扩展阅读:维生素D与肠道菌群的互作
★ 维生素 B12 和叶酸
维生素 B12 的需求量
0 ~ 6 个月为 0.4 微克/天,
6 ~ 不到 12 个月为 0.5 至 0.8 微克/天,
12 ~ 36 个月以下为 0.6 至 1 微克/天。
叶酸的需求量
EFSA 推荐:
0 ~ 6 个月的叶酸营养需求为 65 微克/天,
6 ~ 12 个月婴儿的叶酸摄入量为 80 微克/天,
12 ~ 36 个月以下的需求量为100微克/天;
1-17 岁儿童的叶酸 (FA) 摄入量上限已确定为 200 - 800 微克/天。
叶酸和维生素B12的作用
叶酸和维生素 B12(钴胺素)作为参与广泛生物过程的辅助底物和辅助因子发挥着重要作用,例如核酸合成、糖酵解、糖异生和氨基酸代谢。
此外,叶酸和维生素 B12 以及单碳代谢循环所需的其他微量营养素辅助因子的状况可能会影响 DNA 甲基化,从而对健康产生长期影响。
叶酸——必须,但不要过量
众所周知,怀孕期间缺乏叶酸会导致后代出现神经管缺陷的风险更高。然而,高剂量的叶酸与更好的状态无关,与母亲或后代无关;事实上,怀孕期间摄入量高于 400 微克/天并没有明显的好处。母乳喂养期间补充叶酸可导致母乳总叶酸适度增加。
在儿童中,叶酸缺乏与认知发育受损以及腹泻和呼吸系统疾病增加相关;然而,补充叶酸对于减少这些病症并没有明显帮助。
过量摄入叶酸可能会产生潜在的不利影响,包括几种疾病(例如癌症、神经系统疾病、生长综合征、呼吸系统疾病和多发性硬化症)的发病率增加。
目前,由于食用补充剂或强化食品,很多欧洲儿童摄入大量叶酸;目前尚不清楚这些摄入量是否会造成伤害,尤其是在早期发育过程中,而许多组织中正在发生大量表观遗传变化。
缺乏维生素B12有什么影响?
当母亲的维生素B12状况不佳时,母乳中的含量会降低,会影响后代维生素B12的状态。维生素 B12 对中枢神经系统的代谢和维持至关重要,与叶酸一起在同型半胱氨酸代谢和髓磷脂的保护中起着关键作用。因此,维生素 B12 缺乏会导致覆盖颅神经、脊神经和周围神经的髓鞘受损,从而导致神经精神疾病的发展。
B族维生素缺乏影响肠道菌群
通过基因组重建和预测,针对几种B族维生素,预测整个微生物群落的代谢表型,发现微生物群落中有相当一部分是辅助营养物种(它们无法自己合成某些生命所需的化学物质,需要从外部环境中获取这些物质才能生存),它们的生存完全依赖于从饮食和/或原养型微生物中获取一种或多种B族维生素,通过特定的拯救途径(一种代谢途径,通过这种途径,微生物可以从外部环境或其他微生物的代谢产物中回收利用某些生命所需的化学物质,以满足自身生存所需)来实现。
膳食摄入影响:
母体甲基供体的摄入(胆碱、甜菜碱、叶酸、蛋氨酸)会改变其后代的DNA甲基化。观察到这种摄入量,特别是在围孕期,会影响婴儿口腔中与代谢、生长、食欲调节和维持 DNA 甲基化反应相关的基因的 DNA 甲基化。
细菌合成影响:
除了膳食摄入外,细菌叶酸生物合成也备受关注。细菌叶酸生物合成可以提供额外的叶酸来源,对健康结果和/或 DNA 甲基化具有重要意义。
在体外结肠模型中,研究发现补充甲钴胺和乳清可以提高厚壁菌门和拟杆菌属的比例,同时减少变形杆菌属的数量,其中包括一些病原体,如大肠杆菌(Escherichia)和志贺氏菌属(Shigella)等,以及假单胞菌属(Pseudomonas)。此外,研究还发现甲钴胺可以促进肠道细菌对脂质、萜类化合物和聚酮化合物的代谢,诱导外源性物质的降解,抑制转录因子和次级代谢产物(如维生素 B12)的合成。
扩展阅读:如何解读肠道菌群检测报告中的维生素指标?
B族维生素与肠道菌群互作
02
微生物群和儿童生长
▼ 新生儿肠道菌群
新生儿肠道菌群的建立及发育
新生儿的肠道菌群既直接来自母亲,也来自分娩后的环境。微生物组在生命的头几个月经历动态演替和成熟,这一过程伴随着身体指标以及器官和神经认知发育的快速变化。
新研究结果强调母乳喂养和婴儿饮食会影响肠道微生物组成和功能。一项使用宏基因组鸟枪法测序的综合研究表明,停止母乳喂养(而不是引入固体食物),可以推动婴儿肠道微生物组的功能成熟,使其接近成人状态。
新生儿肠道菌群的影响因素
新生儿微生物组和免疫系统的不成熟似乎与肠道感染的易感性增加有关,特别是在 LMIC(中低收入国家) 环境中。虽然新生儿获得微生物群的时间各不相同,但多次接触,包括分娩方式、母婴饮食、药物、获得安全水和卫生设施以及多种宿主因素,是微生物群组成的主要决定因素。
母乳对婴儿的发育和成熟起着重要作用,微生物组在断奶时进入过渡阶段,此时微生物组会发生其他变化。
▼ 儿童生长
儿童营养不良和生长障碍是由膳食摄入不足和炎症之间复杂的相互作用驱动的,炎症通常是持续和/或反复感染和慢性疾病(包括镰状细胞病、艾滋病毒、先天性心脏病、心理障碍和内分泌或代谢疾病)的结果。
肠病是营养不良的一个重要驱动因素
肠病可能是肠病原体相关性腹泻病的结果,这在 LMIC 环境中的儿童中很常见,并且与死亡率、生长迟缓和认知发育不良的风险较高有关。
而这些环境中的许多儿童在存在或不存在已知肠病原体的情况下患有无症状肠病。这种肠病与非特异性持续粪口污染、反复肠道感染和小肠细菌过度生长 (SIBO) 有关。这种肠病与其他慢性肠道炎症有一些相似之处,包括克罗恩病和溃疡性结肠炎。它与发育迟缓密切相关,可能通过营养吸收不良和食欲抑制间接影响生长,并通过生长激素-胰岛素样生长因子 1 (IGF-1) 轴直接影响生长。
肠道通透性增加也会对发育产生负面影响
肠屏障功能障碍和肠道通透性增加可能导致微生物和/或微生物产物易位,从而激活先天免疫反应并促进全身炎症,从而对生长产生负面影响。
扩展阅读:什么是肠漏综合征,它如何影响健康?
▼ 肠道菌群和儿童成长
肠道微生物群会影响多种宿主功能,包括代谢调节和信号传导,通过获取膳食营养素和微生物群衍生的代谢物、免疫耐受和对病原体的抵抗力、昼夜节律以及与儿童健康成长相关的其他途径。
肠道菌群失调可能影响儿童生长发育
由于疾病、环境或药物暴露或其他损害而破坏微生物组的正常多样性和组成,可能导致生态失调,这是一种以致病菌大量繁殖、共生体丧失和多样性丧失为特征的状态。在一些人群中,生态失调与肥胖、2 型糖尿病、肝脂肪变性和肠道疾病有关。在儿童和部分人群中,生态失调与生长和神经认知发育不良以及反复感染、免疫力改变和炎症增加有关。
与营养良好的儿童相比,营养不良的儿童拥有“不太成熟”的肠道菌群,其多样性较低。生态失调导致营养提取效率低下、吸收不良、易患肠杆菌科等侵袭性疾病和肠道炎症,从而影响生长。
肠道微生物群与发育迟缓之间存在密切关联,表明存在因果机制
谷禾健康与长沙妇幼儿童保健中心实验室合作发表的临床研究,揭示了肠道微生物群对患有严重急性营养不良 (SAM) 等严重儿科病理状况的儿童的重要性;临床诊断为生长发育迟缓 (FTT) 的受试者和正常生长正常的早产受试者 (NFTT-pre) 在不同年龄段表现出明显的肠道菌群发育轨迹中断,并且其α多样性的发展以及观察到的 OTU 和 Shannon 指数不足,尤其是在具有 FTT 的受试者中。
此外,与正常相比,FTT组中细菌如拟杆菌、双歧杆菌、链球菌和大多数年龄歧视性细菌分类群的顺序定殖和富集及其微生物功能紊乱。我们的研究结果表明,发育迟缓的婴儿肠道菌群发育不全,具有潜在的临床和实践意义。

▼ 基于菌群改善儿童生长
肠道菌群失调还与共生微生物的易位和系统传播以及对病原体的易感性有关。此外,共生细菌抵抗肠道炎症的功能能力降低,如产生短链脂肪酸和色氨酸分解代谢配体(驱动芳烃受体激活),可导致肠道炎症。
恢复肠道菌群稳态,可促进儿童生长发育
共生菌还维持先天性淋巴样细胞,这是白细胞介素IL-22 的主要来源,IL-22 可刺激抗菌肽,帮助防止病原菌的微生物移位和入侵。恢复稳态微生物组和相关代谢物,有可能逆转与生态失调相关的表型,并促进儿童的生长发育。
确定肠道微生物群落结构和功能的变化(包括确定它们与疾病的因果关系)以制定有效的干预措施,对恢复肠道微生物群落结构并改善健康生长发育至关重要。
确定可以在怀孕、婴儿期和儿童期实施的干预措施,以预防或改善这些导致生长发育不良的驱动因素,对于改善短期和长期健康与发育至关重要。
扩展阅读:
发育迟缓/营养不良不容忽视,问题很有可能在肠道
真实案例 | 儿童发育迟缓肠道菌群检测的应用
03
怀孕和分娩结果
怀孕期间母体肠道菌群的组成和功能似乎与出生结局密切相关,包括体重和胎龄。在健康的非妊娠成人中,肠道微生物群由相对稳定的种群组成,主要由拟杆菌门、厚壁菌门、放线菌门、变形菌门和疣微菌门组成。微生物组的组成和多样性在怀孕期间发生了变化。例如,在怀孕期间,肠道微生物群 α 多样性和产丁酸菌减少,而双歧杆菌、变形菌和产乳酸菌增加。
最近对来自刚果、印度、巴基斯坦和危地马拉的孕妇进行的一项纵向研究表明,怀孕期间肠道微生物群的个体属和 α 多样性(丰富度)有所减少。
妊娠期肠道菌群与新生儿生长关联
最近进行了一项研究,以了解津巴布韦农村地区妊娠期肠道微生物群分类群与代谢功能对胎龄、出生体重和新生儿生长的关联。
结果证明,抗性淀粉降解细菌,主要是瘤胃球菌科、毛螺菌科和真细菌科,是主要的肠道类群,并且是出生体重、新生儿生长和胎龄的重要预测因子。
此外,这项研究表明,与淀粉和能量代谢、信号和维生素 B 代谢相关的细菌功能,与出生体重增加有关。这些结果表明,非洲农村地区母亲食用富含淀粉的饮食的饮食模式,可能会推动选择影响婴儿健康和成长的物种。
扩展阅读:肠道核心菌属——毛螺菌属(Lachnospira)
肠道菌群变化分别与妊娠糖尿病和高脂血症有关
谷禾健康与江南大学食品科学与技术国家重点实验室合作的临床研究成果表明妊娠糖尿病 (GDM) 通常与高脂血症合并症有关。改变的人类肠道微生物群分别与妊娠糖尿病和高脂血症有关,但与合并症无关。发现链球菌(Streptococcus)、粪杆菌(Faecalibacterium)、韦荣球菌(Veillonella)、普雷沃氏菌(Prevotella)、嗜血杆菌(Haemophilus)和放线菌( Actinomyces )在糖尿病加高脂血症人群中显着更高。此外,几种细菌与患有妊娠糖尿病和高脂血症的参与者的空腹血糖和血脂水平相关。
扩展阅读:肠道重要基石菌属——普雷沃氏菌属 Prevotella
人类肠道核心菌属——韦荣氏球菌属(Veillonella)
母体微生物群的干预:益生菌
针对母体微生物群的干预措施有可能显着影响婴儿健康,因为孕期生态失调和母体暴露会影响微生物群的建立、免疫发育和代谢健康。正在评估妊娠期膳食补充益生菌(对宿主健康有益的活微生物),以预防妊娠相关并发症和不良出生结果,包括早产和极低出生体重。
一些数据表明,益生菌对孕妇或哺乳期妇女在治疗妊娠糖尿病 (GDM)、B族链球菌定植和乳腺炎方面具有有益作用。
鉴于已知的安全性,益生菌作为妊娠干预措施特别有吸引力。然而,迄今为止的研究还没有定论。在新西兰、芬兰、丹麦、瑞典、澳大利亚、伊朗和我国的女性中,补充各种益生菌和混合物(包括乳酸杆菌、链球菌和双歧杆菌菌株)对出生人体测量没有影响。但有一些数据表明益生菌单独或联合使用可能与低收入国家早产儿死亡率、坏死性小肠结肠炎和/或新生儿败血症的降低有关。
04
微生物群和儿童干预
新生儿和婴儿是考虑针对微生物组进行干预的关键人群,因为婴儿微生物组在出生后经历快速进化。此外,婴儿期是生长和神经认知发育的关键时期,也是发病率和死亡率最高的时期。
婴儿肠道菌群的定植
来自拟杆菌门和放线菌门的专性厌氧菌会迅速定植婴儿肠道,主要是双歧杆菌属、拟杆菌属和梭菌属,在生命的前 6 个月内,其特点是多样性低。
母体肠道微生物群似乎对婴儿肠道的定植有显着贡献,而阴道和皮肤来源的细菌似乎更短暂,并且不会在新生儿期后持续存在于婴儿肠道中。
婴儿肠道菌群->免疫系统->宿主
婴儿肠道微生物群为免疫系统的发育提供信息,而免疫系统又协调维持宿主-微生物共生的关键特征。因此,肠道微生物组成和代谢的异常可能会破坏正在发育的免疫系统。
母乳喂养->断奶,肠道菌群变化
婴儿期的母乳喂养还通过母乳中微生物种类的直接转移和其他主要成分的调节影响婴儿生长和塑造肠道微生物群,例如人乳低聚糖(HMO – 人类酶无法消化的复合糖),分泌IgA 和抗菌因子。
断奶,即逐渐将固体食物引入婴儿饮食,是婴儿发育的一个重要里程碑。断奶也是肠道菌群快速扩张的时期,包括双歧杆菌、乳杆菌、韦荣球菌(Veillonella)、柯林氏菌(Collinsella)、普雷沃氏菌、粪杆菌属和大肠杆菌属以及参与复杂多糖代谢的其他物种的多样化和扩张。
断奶期微生物群受干扰,可能导致肠道感染的易感性
断奶时微生物群的扩大还与强烈免疫反应的诱导有关,一种“断奶反应”,其特征是与生命后期的免疫成熟和耐受性相关的调节性 T 细胞的扩增。
在小鼠中,断奶期间限制微生物组的成熟会导致免疫发育受损并增加对肠道感染的易感性。此外,在母乳喂养率高且在长时间断奶期间也接受补充饮食的孟加拉国社区队列中,发现了一个独特的“过渡”长双歧杆菌进化枝,它携带利用母乳和食物底物的酶。这种过渡性长双歧杆菌在断奶期间引入固体食物后会扩大,并且在孟加拉国以外的婴儿队列中也得到证实,尽管患病率要低得多。 这些发现表明,底物和混合喂养的持续时间也会影响肠道微生物组的结构和功能。
断奶期过后,肠道菌群高度依赖于饮食习惯
农村地区的儿童表现出拟杆菌门的显着富集和厚壁菌门的枯竭,普雷沃氏菌属的细菌数量独特丰富,显示出利用富含多糖的营养素的能力。
然而,在工业化国家,这些普氏菌肠型不太常见,断奶后微生物组的特征是拟杆菌和瘤胃球菌肠型的存在。
在试图了解微生物群落是如何共同配置的,包括描述组成成员之间的相互作用以及这些群落随着年龄的增长而成熟时,需要较大的样本人群队列,这也是谷禾一直推进的事情。
微生物群是否有一个稳定的架构?
综合众多的研究结果确定了一个由几十个细菌分类群组成的核心“生态群”,这些分类群在孟加拉国、印度和秘鲁的出生队列的健康成员中,在 20 个月及以后表现出一致的协变。研究得出结论,生态群网络是微生物群组织的一个保守的一般特征,建议这样的生态群可以提供一个框架来描述营养不良儿童的生态失调。
我们建议这样的生态群可以用作定量指标,用于定义旨在重新配置肠道微生物群落的靶向干预措施的功效。
05
益生菌、益生元、合生元
婴儿绞痛、反流和便秘常常引起父母的痛苦也是儿科就诊的主要原因。如前所述,母乳喂养婴儿的微生物群通常被认为富含双歧杆菌和乳杆菌等“有益”细菌,以及梭菌等产气细菌的生长减少。
益生菌:罗伊氏乳杆菌DSM 17938减少哭闹
在随机对照试验中,与安慰剂相比,使用罗伊氏乳杆菌(L. reuteri)DSM 17938 治疗绞痛婴儿可显着减少哭闹时间、反流和功能性便秘。
相比之下,报道了与L. reuteri DSM 17938 相比,安慰剂组在治疗 1 个月时的烦躁时间短暂减少和睡眠持续时间更长。这种烦躁增加仅发生在配方奶喂养的婴儿中,而不发生在母乳喂养的婴儿中。
另一项最近的研究评估了L. reuteri DSM 17938 在 1 个月和 3 个月大时通过显着减少哭闹时间来预防绞痛。一般来说,罗伊氏乳杆菌DSM 17938 似乎可以减少患有绞痛的母乳喂养婴儿的哭闹时间,但是,这种益生菌在绞痛配方奶喂养婴儿中的作用需要进一步研究。
同样对于绞痛的预防,使用L. reuteri DSM 17938 似乎是有效的,但这需要在其他研究环境中得到证实。
扩展阅读:认识罗伊氏乳杆菌(Lactobacillus reuteri)
为了促进“有益”细菌的生长,婴儿配方奶粉中添加了特定的益生元,并在临床试验中进行了评估。
益生元:低聚半乳糖降低绞痛和反流的风险
在最近的一项双盲随机对照试验中,摄入补充低聚半乳糖的配方奶显示出与母乳喂养参照组相似的双歧杆菌和乳杆菌发育趋势,并且与接受不含低聚半乳糖的配方奶粉的婴儿相比,降低了绞痛和反流的风险。
合生元:减少哭闹、减轻疾病发作
人们对合生元提供“有益”细菌及其底物的兴趣也越来越大。
与随机分配到安慰剂配方奶粉的对照组相比,给婴儿喂食七种益生菌菌株和低聚果糖的混合物后,婴儿在第 7 天和第 30 天的哭闹时间减少了 50% 以上。
在另一项前瞻性双盲随机对照试验中,评估了含有嗜热链球菌(Streptococcus thermophilus)、保加利亚乳杆菌(L. bulgaricus)和动物双歧杆菌( B. animalis ssp. lactis)的合生酸奶饮料的效果。
与安慰剂相比,乳糖和菊糖对疾病发作(腹泻、上呼吸道感染和发热性疾病)的影响减少了发烧天数。 干预组大便稀便的频率更高,需要照顾孩子的次数也更多,但差异无统计学意义。
注意:
作者强调益生菌的干预并不是适合所有有症状的婴儿,婴儿的肠道菌群变化较快,益生菌及其组合的干预需要充分评估肠道菌群及其功能,了解其肠道菌群网络结构下,选择对应症状的干预方式才能确保安全和发挥干预的效果。
总的来说,在得出任何确定的结论之前,需要更多的研究来评估益生元和合生元在这些在不同类型儿童及其整体肠道微生态条件下的作用。
扩展阅读:
如何调节肠道菌群?常见天然物质、益生菌、益生元的介绍
肠道微生物群与健康:探究发酵食品、饮食方式、益生菌和后生元的影响
06
微生物群、益生菌和过敏性疾病
人们还关注肠道菌群失调在过敏表型发生发展中的作用。
肠道菌群 & 过敏性疾病
肠杆菌科/拟杆菌比率↑ -- 食物致敏的风险↑
据报道,在基于人群的加拿大健康婴儿纵向发育 (CHILD) 出生队列研究中,婴儿粪便中低肠道微生物群丰富度和升高的肠杆菌科/拟杆菌比率与随后食物致敏的风险增加有关。
瘤胃球菌科↓
--食物敏感 --特应性湿疹 --炎症性先天免疫反应过度
他们还发现食物敏感的婴儿在 1 岁时瘤胃球菌科的丰度下降。这可能与过敏性疾病高风险婴儿的病例对照研究结果一致,发现瘤胃球菌科的相对丰度较低与未出现任何过敏表现的婴儿相比,随后出现特应性湿疹的婴儿的粪便样本中。
值得注意的是,瘤胃球菌属的相对丰度较低也与炎症性先天免疫反应过度有关。
总的来说,这些发现进一步支持了这样一种假设,即缺乏潜在的免疫调节细菌可能会增加发生过敏表现的风险。由于瘤胃球菌能够降解纤维,并且是成人“核心”微生物组的一部分,未来的研究应该检验其重要性。
扩展阅读:瘤胃球菌属——消化降解关键菌?炎症标志菌?
益生菌 & 肠道菌群
鼠李糖乳杆菌GG -- 产丁酸菌↑
在最近的一项研究中,研究了益生菌对牛奶过敏婴儿肠道微生物组的影响。报道称,添加了鼠李糖乳杆菌GG (LGG) 的深度水解酪蛋白 (EHCF) 配方导致了与丁酸盐生产相关的特定细菌的富集。
丁酸盐是一种已知的结肠细胞底物,与增强肠道完整性有关。与单独使用 EHCF 相比,接受 EHCF + LGG 治疗的婴儿在治疗 6 个月后的丁酸产量呈双峰分布。
已知的丁酸盐生产者,Faecalibacterium,Blautia,Ruminococcus,Roseburia在高丁酸盐样本中富集,而拟杆菌显着减少。与牛奶不耐受的孩子相比,牛奶耐受的孩子Blautia和Roseburia富集。正如作者推测的那样,这些物种可能导致丁酸盐产量增加和肠道完整性增加。
扩展阅读:
肠道核心菌属——经黏液真杆菌属(Blautia),炎症肥胖相关的潜力菌
肠道重要基石菌属——罗氏菌属(Roseburia)
肠道核心菌属——普拉梭菌(Faecalibacterium Prausnitzii),预防炎症的下一代益生菌
母亲摄入益生菌降低孩子发病率
在该团队随后的2份研究中,其中在一项随机对照试验中,与无菌安慰剂牛奶相比,孕妇在围产期摄入含益生菌的低脂发酵牛奶可降低其孩子 2 岁和 6 岁时的湿疹发病率。然而,临床益处似乎与 3 个月或 2 岁时对肠道微生物多样性的影响无关。
由于益生菌仅给予母亲,另一种解释可能是通过影响母乳成分。在婴儿期益生菌随机对照试验的另一项后续研究中,对长期肠道微生物群的建立没有影响, 这与之前的报道一致。
注意:
虽然说荟萃分析报告,怀孕期间、母乳喂养期间和/或给婴儿服用益生菌可降低婴儿湿疹的风险,但证据仍然薄弱。因此,专家机构未能推出具体的指导方针。然而,在考虑所有关键结果时,世界过敏组织现在建议使用益生菌预防有过敏孩子高风险的孕妇和哺乳期母亲以及有高风险患过敏性疾病的婴儿(基于家族史)。
在他们的指南中,他们强调该建议是有条件的并且基于低质量的证据,并不能给出关于最有效的菌株、剂量或治疗的开始和持续时间的具体指导。因此,仍然需要更具体的指南和研究基础。
07
肠易激综合征、克罗恩病和乳糜泻中的肠道微生物群调节
肠易激综合症
在一项评估肠易激综合征儿童低发酵底物饮食的初步研究中,该饮食与腹痛频率和严重程度的降低显著相关。与无反应者相比,对治疗有反应的儿童在基线和干预期间似乎具有不同的粪便微生物组。
在一项更大的、双盲、随机、交叉研究中,同一组使用 16S 测序研究了低发酵低聚糖、二糖、单糖和多元醇 (FODMAP) 饮食对肠易激综合症儿童的临床结果和肠道微生物组成的影响。
低 FODMAP 饮食减少了腹痛,并且对饮食有反应的儿童的微生物群具有更强的糖分解能力。作者建议,鉴定具有更强糖分解能力的微生物群可能作为预测对低 FODMAP 饮食反应的生物标志物。
克罗恩病
肠道微生物群环境的变化被认为是克罗恩病患者纯肠内营养治疗特性的中介。令人惊讶的是,与没有炎症性肠病家族史的健康对照相比,克罗恩病患儿在纯肠内营养过程中肠道微生物多样性、普拉梭菌和丁酸盐浓度有所降低。
当参与者恢复正常饮食时,这后来又恢复到治疗前的水平。伴随着这种假定的“不健康”微生物群,矛盾的是临床结果得到改善,结肠炎症标志物减少。然而,这些发现的相关性需要进一步阐明。
乳糜泻
在乳糜泻中,坚持严格的无麸质饮食 (GFD) 有时很困难,患者可能仍会出现临床症状和营养缺乏,随后持续发炎和肠道菌群失调。
由于特定的益生菌已被证明可以减轻炎症,因此在一项双盲探索性试验中,新诊断出患有乳糜泻的儿童被随机分配到摄入长双歧杆菌CECT 7347 或安慰剂组 3 个月。无论治疗如何,对 GFD 的依从性与生长参数呈正相关,与安慰剂组相比,益生菌组的身高有所增加。此外,益生菌处理减少了脆弱拟杆菌的数量组和分泌型 IgA。
在另一项评估两种益生菌短双歧杆菌菌株对 GFD 患儿影响的随机对照试验中,与安慰剂相比,干预减少了炎性细胞因子 TNFα 的产生。
总的来说,这些研究表明益生菌对患有乳糜泻的儿童可能有益,但需要在更大规模的试验中验证。
扩展阅读:双歧杆菌:长双歧杆菌
08
微生物群和儿童代谢消化
青年糖尿病环境决定因素 (TEDDY) 研究最近的一份报告中,该研究包括芬兰、瑞典、德国和美国患 1 型糖尿病的高风险儿童,肠道的组成和多样性都存在很大差异。即使在这个具有同源人类白细胞抗原 (HLA) II 类基因型并因此具有相似遗传风险的人群中,根据地理区域也存在显着差异。
这些差异的根本原因尚不清楚,因为即使在对早年生活和饮食变量进行调整后,差异仍然存在。
在同一项前瞻性队列研究中,还检查了早期接触益生菌和膳食可溶性纤维(可能影响肠道微生物群组成和形成免疫反应)与胰岛自身免疫的关系。与后期补充或无益生菌相比,益生菌暴露(≤27 天)与胰岛自身免疫风险降低相关。 相反,儿童早期膳食可溶性纤维的摄入与胰岛自身免疫或 I 型糖尿病无关。未来的研究需要检验这些发现的重要性。
09
结 语
人们一直对肠道菌群失调在影响儿科人群的大量疾病中的作用感兴趣。
儿童生长迟缓和认知发育不良的驱动因素是多方面的,包括饮食摄入量和多样性不足、暴露于反复感染、慢性疾病和肠道病理学,包括肠病和 SIBO。最近的研究表明,肠道菌群失调与发育迟缓之间存在密切关联,表明存在潜在的因果关系。这些研究强调需要确定肠道微生物群落的结构和功能改变,并恢复微生物组稳态和相关代谢物以促进低收入环境或国家儿童的生长发育。
儿童时期的肠道微生物组成高度依赖于饮食习惯。在营养不良的儿童中,与标准营养干预措施(如 RUSF)相比,含有当地可用成分的低热量密度 MDCF 可改善微生物组的成熟度和生长。未来我们需要努力探究不同地理环境和不同饮食习惯下中婴儿期微生物群的多样性,更深入地了解它们与免疫发育和生长的联系。
鉴定具有更高定植效率和临床有效性的适合当地的菌株可能提供巨大的潜力来优化可在怀孕、婴儿期和儿童期实施的干预措施,这可能会导致针对肠道微生物群的治疗和预防策略得到改进,并且也可能成为安全和具体指南的基础。
主要参考文献:
Njunge JM, Walson JL. Microbiota and growth among infants and children in low-income and middle-income settings. Curr Opin Clin Nutr Metab Care. 2023 Mar 6.
Videhult FK, West CE. Nutrition, gut microbiota and child health outcomes. Curr Opin Clin Nutr Metab Care. 2016 May;19(3):208-13.
Cerdó T, Diéguez E, Campoy C. Infant growth, neurodevelopment and gut microbiota during infancy: which nutrients are crucial? Curr Opin Clin Nutr Metab Care. 2019 Nov;22(6):434-441.
WHO. Levels and trends in child malnutrition: key findings of the 2021 edition of the joint child malnutrition estimates. United Nations Children's Fund (UNICEF), World Health Organization, International Bank for Reconstruction and Development/The World Bank. 2021.
Gizaw Z, Yalew AW, Bitew BD, et al. Stunting among children aged 24-59 months and associations with sanitation, enteric infections, and environmental enteric dysfunction in rural northwest Ethiopia. Sci Rep 2022; 12:19293.
West CE, Renz H, Jenmalm MC, et al. The gut microbiota and inflammatory noncommunicable diseases: associations and potentials for gut microbiota therapies. J Allergy Clin Immunol 2015; 135:3–13.
Troesch B, Biesalski HK, Bos R, et al. Increased intake of foods with high nutrient density can help to break the intergenerational cycle of malnutrition and obesity. Nutrients 2015; 7:6016–6037.
Hiltunen H, Löyttyniemi E, Isolauri E, Rautava S. Early nutrition and growth until the corrected age of 2 years in extremely preterm infants. Neonatology 2018; 113:100–107.
Zheng M, Lamb KE, Grimes C, et al. Rapid weight gain during infancy and subsequent adiposity: a systematic review and meta-analysis of evidence. Obes Rev 2018; 19:321–332.
以上是关于肠道微生物群影响眼部健康的主要内容,如果未能解决你的问题,请参考以下文章