重磅综述:人类电生理的脑连接组学
Posted
tags:
篇首语:本文由小常识网(cha138.com)小编为大家整理,主要介绍了重磅综述:人类电生理的脑连接组学相关的知识,希望对你有一定的参考价值。
参考技术A 脑连接组学是一门快速发展的神经科学子学科,可以用来从宏观尺度上检查不同脑区之间的功能和结构连接关系。研究表明,功能性磁共振成像中常见的规范脑连接网络实际上植根于电生理过程。电生理学研究将为分层大脑网络中的信息整合提供可测试的机制模型。总之,电生理学包含一组交叉科学技术和方法,可提供对大脑系统神经动力学的探索。原则上,它们可以就功能通信如何在大脑网络中以生物学方式实现提供独特的见解,从而在广泛的时间范围内实现复杂的行为 。 此综述的目标是解释电生理学方法与连接组学研究之间的相关性。1 简介
脑连接是神经科学中一个年轻而快速发展的分支学科,它已经改变了人类的大脑图谱。 连接组研究起源于21世纪初的核磁共振,在图论等数学工具的推动下,旨在提供对健康和疾病中大脑结构和功能的综合分析 。 电生理功能连通性可以定义为一组描述“跨低级别网络的高级别耦合”的指标。低水平网络是由相互连接的细胞组成,分布在1厘米或更大的皮质上--这种空间尺度在整个大脑中随局部细胞密度、区域深度和该区域内电流的主要方向而变化。因为这种局部回路在功能上是相对同质的,所以我们把它们称为“大脑区域”。高水平的耦合构成了这些局部区域之间的信号相互作用。这些相互作用的区域相隔的距离基本上大于网络中每个区域的空间范围,它们构成了本文提及的高级网络。
电生理技术是历史上第一个测量大脑活动的技术,在基础(人类和动物研究)和临床神经科学中仍然是最容易获得和发表最多的技术。它们由非常多样化的方法组合而成,这些方法随着几十年来传感和计算技术的进步而演变。 它们的特殊优势是:1) 直接评估神经活动的能力,对比间接代谢信号;2) 毫秒级的时间分辨率;3) 从单个细胞到整个大脑的多空间尺度记录;4) 通过神经刺激确定因果效应;以及5) 便携式、可移动仪器的可用性、成本效益和数据质量的日益增长 。
总而言之,电生理学包括一套交叉的科学技术和方法,为研究大脑系统的神经动力学提供了独特的途径。原则上,它们可以对大脑网络中如何在生物学上实现功能性通信提供独特的见解,从而在广泛的时间范围内实现复杂的行为分析 。 我们在这里的目标是解释为什么这些独特的特性使电生理方法特别适用于脑连接组研究。
2 电生理连接的度量
2.1 电生理数据类型
大脑区域之间的电生理高级连接的测量必须提供 1)高保真度,即足够的信噪比(SNR),以准确表征来自不同大脑区域的信号之间的统计依赖性;2) 足够的空间分辨率,以确保区域之间的连通性估计不会因从一个区域到另一个区域的虚假信号交互(“泄漏”或“串扰”)而显着降低。考虑到这两点,电生理测量可以分为两类:
(1) 非侵入性方法 包括脑电图 (EEG) 和脑磁图 (EMG)。前者测量大脑中波动电流产生的头皮表面的电位差,后者测量相同电流波动产生的相应磁感应。
(2) 侵入性测量 通常统称为颅内脑电图 (iEEG),范围从皮层电图 (ECoG)到更深结构的深度电极。电极参考位置的选择通常决定了进行测量的神经元群体的大小。测量结果通常反映了来自皮层锥体细胞 (类似于MEG/EEG) 的 LFP,这些细胞总和超过了数千个神经元。
由于颅外传感器远离脑源,脑磁图和脑电图具有较低的信噪比(尤其是在高频下)。与EEG相比,MEG提供更高的空间精度,因为它对头部组织的几何形状和电导不太敏感。MEG也不太容易受到生物伪影的影响。然而,MEG 的购买和运营成本也更高,因此更难获得。传感技术的重大进步有望提供新的、更灵活和负担得起的 MEG 仪器,这些仪器最近被证明对连通性测量有效。
2.2 电生理信号连通性评估方法
从广义上讲,电生理连接指标可以分为两类,频带内和频带间。目前流行的两类频带内连通性度量:固定相位关系和幅度相关度量。这些不同的技术被认为可以深入了解两种不同的功能连接模式。对于频带间测量,存在三种典型的技术系列:相位-相位、幅度-幅度和相位幅度耦合,后者是最常用的 。 图1中展示了常规的基于生理电信号的脑连接构造步骤。
图1处理电生理数据以得出电生理连接组测量的基本方法
与所有类型的生物信号分析一样,对电生理连接的最大威胁源于数据质量的固有限制,最值得注意的是空间分辨率和信号泄漏有关——尤其是对于 MEG/EEG。近年来,已经引入了可靠且稳健的方法来减轻泄漏。其中大多数依赖于这样的想法,即泄漏必然表现为具有零时滞的信号之间的关系。在探测信号之间的固定相位关系时,可以轻松消除这种零滞后效应——例如,仅采用相干计算的虚部,或通过使用相位滞后指数。除了上面定义的一类指标,研究者还开发了许多有向指标,例如格兰杰因果、部分定向相干性和动态因果建模。 这些指标利用电生理测量的高时间分辨率来推断两个区域之间信息流的平均(在某个时间窗口内)方向。
2.3 面向动态时序连接
上述连接性度量通常应用于许多分钟或几个小时的数据,并且被称为“静态”连接体。事实上,情况并非如此,因为大脑必须在快速(毫秒)的时间尺度上持续形成和分解网络,以回应不断变化的认知和行为需求。
2.3.1 滑动窗方法
在最简单的层面上,动态连接可以通过“滑动”窗口计算。一个关键点是这种技术提供的效用取决于窗口的长度。反过来,这取决于人们在多大程度上可以在短时间内获得可靠的连通性度量,而这本身取决于信号中自由度的数量。一个信号的时间自由度 n = 2 Bw D ,其中 Bw 是信号带宽, D 是窗口的时间宽度。虽然fMRI信号的带宽为~ 0.25 Hz,但电生理信号的名义带宽至少为100 Hz。这意味着,在电生理学中,基于滑动窗口的连接测量的时间窗口比fMRI短约400倍。这反过来又使电生理学成为动态功能连接测量的首选技术。在实践中,电生理信号在不同波段包含不同的特征,人们通常会考虑计算窄带信号(如alpha、beta、gamma波段)的连通性。这意味着fMRI在时间分辨率上的改善并没有那么显著。然而,即使对于最窄的波段(例如8-13 Hz alpha波段),带宽仍然保持在5 Hz,在时间分辨率上比fMRI至少提高20倍。
然而,尽管电生理信号的带宽很高,滑动窗口宽度的选择仍然是一个有趣问题。人们真的希望窗口宽度与大脑中网络波动的时间尺度相匹配。然而,在实践中,这几乎肯定是未知的,并且可能在实验过程中发生变化。同样,对于不同的网络,它可能是不同的,随着年龄或参与者的病理状态而变化。也有可能,连通性波动的时间尺度可能太短,无法有效测量窗口内的连通性(例如,对于alpha波段,1秒的窗口,与认知加工相比仍然很长,只包含10个自由度)。由于这些原因,虽然滑动窗口仍然是一个有用的和概念上直接的工具,但很可能其他方法可以更好地利用电生理学提供的高时间分辨率。
2.3.2 除滑动窗方法之外
许多技术试图“时刻”检查连通性,即在电生理时间过程中获得每个样本的功能连通性估计。一种可用的技术是相位差导数 (PDD)。简而言之,PDD探测固定相位关系的存在,采集来自远端区域的信号的瞬时相位,并随时间测量它们之间的差异。如果差分导数为零,则暗示瞬态固定相位关系。近年来,基于隐马尔可夫开发的一种技术能够回避窗口问题。该方法假设电生理数据由一系列相互排斥的隐藏“状态”控制。这意味着在任何一个时间点,大脑都可以说是处于一种特定的状态。在未平均或静止状态中,PDD和类似指标往往是不稳定的,并且最终会在时间窗口上取平均值,这最终导致滑动窗口面临同样的问题。然而,在基于任务的研究中,假设相同的实验范式重复多次,PDD 可以在试验中平均。
一种基于隐马尔可夫建模的技术(HMM)能够回避窗口问题。迄今为止,该技术主要应用于MEG,但最近的论文已将其用于EEG和fMRI。HMM假设电生理数据由一系列相互排斥的隐藏“状态”控制。这意味着在任何一个时间点,大脑都可以说是处于一种特定的状态。在最简单的形式中,HMM可以描述单个电生理时间过程中的状态。每个状态都可以用电生理数据的高斯分布来描述。使用这种无监督的方法,大脑何时进入或离开特定状态的识别是自动化的。因为 HMM以数据驱动的方式自动选择时间窗口。
3 利用正在进行的电生理活动来定义电生理连接组
许多常见的电生理分析本身无法提供对大脑行为关系的全面机制理解。电生理测量通常重复多次,并且在试验中对数据进行平均,以检测相对于“基线”参考期的可能影响 。 在大多数电生理研究中,基线被丢弃,将持续的大脑动力学视为“噪音”。在这里,我们主张充分利用,而不是“纠正”,正在进行的神经过程及其空间组织对电生理记录的贡献。与任务相关的连通性变化通常将正在进行的电生理过程视为“噪音”。 同样重要的是,研究少数与任务相关的传感器的选择方法忽略了电生理数据的分布式空间组织 。 3.1小节详细阐述了正在进行的电生理活动的空间组织(即跨区域对的连接强度的全脑模式),并讨论其行为意义。3.2小节简要回顾了有关正在进行的活动动态的最新证据。
3.1 持续的电生理活动具有内在的时空组织
3.1.1 颅内电生理学中的内在空间组织
尽管颅内研究通常缺乏全面描述内在连接网络所需的全脑覆盖,但个别研究证实了特定内在连接网络的存在 。 一项研究报告表明,在所有规范频带中,组级 fMRI 连接组与汇集的全脑ECoG连接组之间存在适度的关联。值得注意的是,尽管许多寻求与 fMRI 衍生的功能连接相似性的研究都集中在高伽马功率的缓慢共波上,但上述研究扩展到其他振荡频率的幅度耦合以及振荡相位的测量。总之,人类 iEEG 研究提供了关于存在跨振荡频率和连接测量的持续电生理连接的内在空间组织的信心,并且还为 fMRI 中经常报告的空间网络组织提供支持。
图2 电生理数据中内在的全脑连接组织。A)在源空间MEG幅度耦合中通过基于种子的连接观察到的感觉和运动的内在脑连接。光谱图(右)表明alpha和beta波段振荡对这些内在网络的贡献很大;B) MEG中特定频带的振荡幅度的内在脑连接(显示了四个作为示例),包括感觉/运动以及高阶网络;C)连接强度在 fMRI 和颅内电生理学(ECoG 幅度耦合)之间存在空间关联。对于所有频段,这种相关性的强度约为 0.35;D)在 fMRI 和同时记录的头皮脑电图(相位耦合)之间观察到类似的连接强度的空间关联。左侧散点图显示了 beta 波段的示例,其中每个数据点来自连接组的一个区域对,平均跨受试者中以相似的效应大小重现。
3.1.2 颅外电生理信号的内在空间组织
有了对内在空间组织建立的信心,我们转向全脑连接组的MEG和 EEG 源空间研究。许多 MEG 幅度耦合研究为使用基于种子的相关性提供了感觉和运动趋同的证据。虽然其中一些研究使用宽带信号,但那些专注于不同频段的研究通常报告 α 和β 频段在反映 内在脑连接方面占主导地位。此外,虽然幅度耦合一直是MEG 静息状态连接组研究中更常用的连接模式,但 MEG 相位耦合显示出由内在脑连接锚定的类似空间分布。 尽管与 MEG 相比,EEG 对体积传导的敏感性更强,但 EEG 同样有力地反映了连接组的内在空间组织 。
图3 功能网络的毫秒动态。A)应用于静息状态MEG的隐马尔可夫模型(HMM)提取数据。每个状态都由特定的地形决定。这些状态图类似于fMRI通常观察到的典型内在连接网络 (ICN)。B)与 HMM 状态相关的时间尺度显示在面板A中;C)“重放”是大脑自发地重新审视最近获得的信息以例如巩固记忆的过程。这些重播事件与特定 HMM 状态发生概率的改变有关。左图显示了“重放”事件期间 HMM 状态发生概率的变化。右侧的地图显示了在回放期间更有可能表达的四个大脑网络,其中包括默认模式和顶叶阿尔法网络。
3.1.3 跨认知状态的内在电生理连接组的稳定性
大规模连通性的内在空间组织的一个关键特征是其认知上下文的相对独立性。这种对认知环境的不敏感性在fMRI中得到了很好的量化,表明大脑的fMRI 衍生的时间平均连接组组织的特定任务变化很小。然而,与 BOLD 信号的非周期性慢速波动相比,基于振荡的功能连接可以很好地支持认知过程所需的数十到数百毫秒的快速时间尺度上的远程通信。这种能力是否会导致认知环境对电生理 FC 组织进行更强的重构?诸如上述讨论的电生理连接组研究通常侧重于无任务静息状态,很少有电生理连接组研究定量比较认知状态。
一项这样的研究分析了不同唤醒水平和日常活动的一天 iEEG 记录。源自 100秒和更长周期的幅度和相位耦合在昼夜循环中显示出一致的空间组织。一项使用传感器级脑电图的相关研究确定了振幅和相位耦合组织在不同睡眠阶段和觉醒的高度空间相关性。源空间中的EEG研究表明,在对不同任务(静止状态、视频观看和闪烁光栅)进行几分钟计算时,相位耦合在空间上是一致的,并且跨频带具有相似的模块化组织。相位和幅度耦合揭示了跨认知状态的高度相似、很大程度上与状态无关的空间分量。这种空间组织在所有频带之间共享。
总的来说,这些研究表明,功能连接的空间组织在认知状态(包括觉醒水平、静息清醒和具有不同认知需求的任务期)上基本稳定,即它本质上主要是内在的。该组织在很大程度上也是跨频段共享的。因此,电生理连接组的动态变化,包括那些自发发生的、由任务环境引发的或由刺激引起的变化,应该根据相对稳定的内在组织的信息偏离来研究 。
3.2 持续的活动在快速的时间尺度上动态变化
连接性随时间变化的现象已得到充分证实。虽然连接的静止状态波动很明显,但有时很难(甚至不可能)将这些波动与行为联系起来 。 奥尼尔等人使用滑动窗口来演示电生理连接如何随着运动任务而变化。这项工作采用了一种基于典型相关性的方法,能够检测感觉运动系统中的“子网络”。Neill 等人使用 6 秒滑动窗口测量了完整的连接组矩阵,并展示了 Sternberg 工作记忆任务期间网络的形成和分解。 这些研究开始表明,功能连接的完整动态方法为任务诱发动力学提供了新的见解 。
使用隐马尔可夫模型可能会消除滑动窗口(和类似)方法的局限性 。 在 Baker 等人的早期论文中,这种方法被用来揭示大脑状态的复发,这些状态被证明存在于几百毫秒的时间尺度上。Vidaurre 等人表明可以从正在进行的电生理数据中提取规范的 ICN(运动、视觉、默认模式)。重要的是,这些网络再次被证明可以在快速(<100ms)的时间尺度上进行调制。这些研究表明,规范ICN的表达可能会在比以前想象的更快的时间尺度上发展。
测量网络动力学毫秒波动的能力引出了一个问题,即是否可以使用相同的方法来理解电生理数据的持续时空特征如何与任务相交 。 Higgins 及其同事最近的工作解决了这个问题。作者使用 HMM 来模拟自发记忆“重放”期间的网络波动。回放是与特定项目相关的神经活动自发启动以巩固记忆的过程。回放事件通常在默认模式和顶叶 alpha 网络的激活期间选择性地发生——这两个网络已知与内向注意力相关。 这些发现提供了迄今为止最清晰的指示,表明正在进行的电生理网络活动如何被动态和选择性地调节以支持认知处理 。
综上所述,电生理学为以毫秒级时间和高空间精度标测动态连接体提供了最佳途径。结合对神经生理学相互作用的有意义的测量,它有助于更好地表征静息状态无任务数据。此外,电生理学还有助于更深入地理解任务诱发事件与正在进行的大脑活动之间的关系 。
4 有意义的电生理信号的频率带宽是多少?
电生理信号的毫秒级分辨率是他们最大的神经科学资产。信息论的一个主要结果是,信号分量以采样频率的一半的速度演化,就可以传达有意义的内容。当前电生理学硬件的数字化采样率可以高达每通道几十kHz。这是否意味着高达10kHz的大规模大脑信号波动传达了对识别连接组相互作用有意义的信息位 。
在特定环境中测量特定生物系统的每一种仪器都容易受到噪声的影响。噪声表征经常被随便忽视,因为它具有挑战性或根本不切实际。在我们的领域中,MEG系统最适合仔细表征环境和仪器噪声条件。运行“空房间”测量确实被认为是一种很好的做法,即在每个实验会话周围没有参与者在 MEG 传感器阵列下的情况下,以捕获可能在会话之间发生变化的噪声条件的导数,此类“干”数据运行有助于表征技术本底噪声及其频谱时间结构。
对于EEG,“空房间”条件是不切实际的,因为电极信号需要直接接触导电介质,即头皮或精心制作的导电体模设置。因此,截止频率和采样率通常是特殊定义的,通常设置在数百赫兹的范围内。这既不完全严谨也不令人满意,而只是举例说明了实验神经科学的某些方面如何仍然受到实践的指导。
考虑1 kHz采样的数据,这是该领域常见的范围。因此,理论上可用于信号分析的最大频率为500 Hz,实际上约为 250-300 Hz,这通常由仪器的附加抗混叠硬件滤波器强加。一个 250Hz 的大脑信号频带代表了一个由慢到快波动的广阔领域,以表征 电生理连接 组。从电气工程的角度来看,电生理数据因此被认为是 宽带 信号。有经验证据表明,头皮和皮质记录可以捕获与复杂的人类行为或临床症状有意义相关的快速(高频)信号。例如,外部感觉信号的神经夹带是一种强大的实验方法,可以通过在高达100 Hz左右的快速频率下特别提高它们的信噪比。刺激事件也可以诱发100 Hz以上的高频振荡突发并且由癫痫脑自发产生。这种快速信号是否在大脑网络的区域间通信中发挥作用是一个积极研究的问题。
总之,宽带信号可以实现丰富多样的信息通道。这意味着神经信息位可以通过不同的信息通道(例如限制在窄频带内的振荡信号)和/或通过更复杂的信号编码形式(例如相位幅度、交叉频率)在区域之间并行传输互动或以上所有。这些考虑对于产生可测试的机械假设以理解定义功能连接组的电生理信号相互作用的性质具有深远的意义 。
5 总结
本文总结了跨电生理学和功能磁共振的连通性在空间和时间上的收敛,它们不受逆问题的影响。我们还强调了电生理连接与个体内部和个体之间的行为的关联,以及与认知过程(如记忆巩固)相关的快速时变连接动力学,这些进一步支持了源定位电生理连接的重要性。使用血流动力学信号在很大程度上无法获得如此快速的连接组状态变化。此外,电生理和功能磁共振连接可能反映部分不重叠的神经和生理现象。功能性磁共振被概念化为由血流动力学反应平滑的电生理活动。然而,经过优化以在快速或慢速时间尺度上进行通信的神经群体和神经束可能分别通过电生理和功能磁共振测量得到更大的权重,并且功能磁共振连接可能容易受到跨区域血管需求的影响 。
最后,我们认为全脑电生理连接组学是基础和临床神经科学研究的机会。我们希望当前的观点和立场能够激发人们的信念,以充分利用人类大脑的分布式持续电生理中未知的财富。
参考文献:
Connectomics of human electrophysiology
干货 | 浅谈代谢组学常用数据库类型
关
注
点击“迈维代谢MetWare”,
了解更多代谢组前沿
代谢组是指某一生物或细胞、组织在一特定生理时期内所有的低分子量代谢产物的集合,主要是指分子量小于1000 Da的内源性小分子。
根据不同的理化属性可以将代谢组学所包含的物质主要分为氨基酸类(amino acid)、肽类(peptide)、碳水化合物类(carbohydrate)、能量类(energy)、脂类(lipid)、核苷酸(nucleotide)、维生素和辅助因子(cofactors andvitamins)及外源化合物(xenobiotics)。
面对种类如此繁多复杂的物质,代谢物鉴定成为代谢组学研究的重点,也是目前最主要的技术瓶颈。代谢物的鉴定高度依赖于代谢物标准品库,今天小编就主要介绍下代谢组学常用数据库。
HMDB即人类代谢组数据库( http://www.hmdb.ca/)于2007年首次发布,目前是世界上最大、最全面的特定生物体代谢组学数据库。该数据库包含或链接三种数据:化学数据、临床数据和分子生物学/生物化学数据。数据库中含有114162个代谢物条目,包括水溶性和脂溶性代谢物,以及被视为丰富(> 1 uM)或相对稀有(<1 nM)的代谢物,涉及25770个代谢途径、18192个代谢反应。

METLIN(https://metlin.scripps.edu/)起源于表征已知代谢物的数据库,目前已扩展为用于鉴定已知和未知代谢物及其他化学实体的技术平台。该数据库超过一百万个分子,包括脂质、氨基酸、碳水化合物、毒素、小肽和天然产物等。METLIN的高分辨率串联质谱(MS/MS)数据库来自于标准品及其标记的稳定同位素类似物生成的数据,在鉴定代谢物过程中起着关键作用。并且METLIN可通过MS/MS数据和片段相似度搜索功能识别未知代谢物。

MassBank(http://www.massbank.jp/),一个高质量质谱数据库,旨在公开分享从代谢物的化学标准品得到的质谱图以方便用户进行代谢物的鉴定。MassBank包含了代谢物的质谱信息以及采集情况,这些信息来自于不同的质谱仪设置,包括不同的电离技术例如ESI(60%)、EI(31%)、CI(2%)、APCI(1.6%)以及MALDI。
MetaboLights(https://www.ebi.ac.uk/metabolights/)是代谢组学实验和衍生物信息的数据库。该数据库包含了不同物种、不同技术的数据,涵盖了代谢物结构、参考光谱、生物学作用、位置和浓度,以及代谢实验数据。
Metabolomics Workbench数据库(www.metabolomicsworkbench.org/)跨各种物种、实验平台、代谢物标准品、代谢物结构和其它资源。它提供了一个计算平台,可以集成、分析、跟踪、存放和传播来自各种代谢组学研究的大量异构数据,包括质谱(MS)和核磁共振谱(NMR)数据,涵盖20多种不同物种,主要类别包括人类、哺乳动物、植物、昆虫、无脊椎动物和微生物。此外,还提供了一系列基于MS和NMR的代谢物类别、样品类型研究方案,以及代谢物结构数据库。

KEGG数据库(https://www.genome.jp/kegg/ligand.html)是京都基因及基因组百科全书,在分子和更高水平上为基因和基因组分配功能性含义是KEGG数据库项目的主要目标。全书收录了生物的所有代谢物的代谢途径,支持对代谢网络的搜寻及代谢途径的映射。与代谢组学相关性大的几个模块包括:KEGG PATHWAY , KEGG DISEASA ,KEGG COMPOUND , KEGG REACTION。
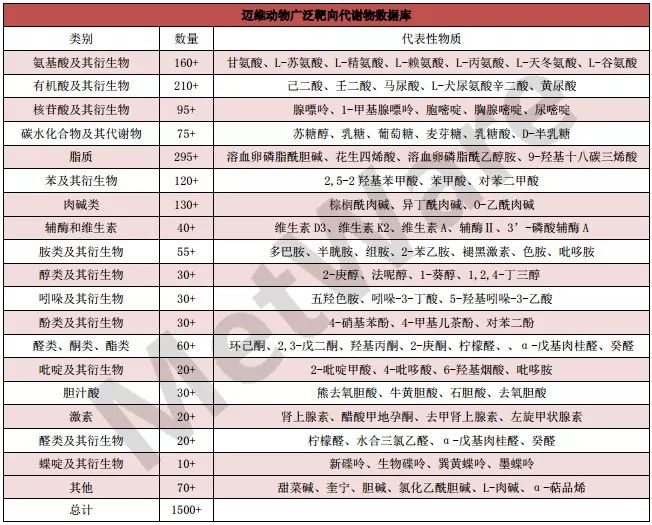
此外,还有其他许多个性化的代谢物数据库及相关软件,包括Reactome、Cyc databases、Lipid Maps、PubChem、LMDB等等。而迈维代谢针对植物、动物建立专属代谢物数据库,涵盖氨基酸、脂质、核苷酸、碳水化合物、维生素和辅助因子、激素等,包含代谢物结构、色谱数据、质谱数据等,旨在更专业的通过代谢组学解决生物学问题。
参考文献
1. Kanehisa,M., Furumichi,M., Tanabe,M., Sato,Y. and Morishima,K. KEGG: new perspectives on genomes, pathways, diseases and drugs. Nucleic Acids Res. 2017, 45, D353–D361.
2. Carlos Guijas, J. Rafael Montenegro-Burke, Xavier Domingo-Almenara, et al. METLIN: A Technology Platform for Identifying Knowns and Unknowns. Anal Chem. 2018, 06; 90(5): 3156–3164.
3. Sud,M., Fahy,E., Cotter,D., et al. Metabolomics Workbench: an international repository for metabolomics data and metadata, metabolite standards, protocols, tutorials and training, and analysis tools. Nucleic Acids Res, 2016, 44, D463–D470.
4. Kale,N.S., Haug,K., Conesa,P., et al. MetaboLights: an open-access database repository for metabolomics data. Curr. Protoc. Bioinformatics. 2016, 53, 14.13.1–14.13.18.
5. David S. Wishart , Yannick Djoumbou Feunang, Ana Marcu1, et al. HMDB 4.0: the human metabolome database for 2018. Nucleic Acids Research. 2018, 46, D608–D617.
★ 迈维产品服务★
|
植 物 产 品 |
植物广泛靶向代谢组 植物初生代谢组 植物次生代谢组 黄酮代谢组 萜类代谢组 生物碱代谢组 花青素检测 木质素小分子途径检测 植物激素检测 类胡萝卜素检测 糖类代谢检测 靶向代谢物检测 挥发性物质检测 |
|
动 物 产 品 |
动物广泛靶向代谢组 动物广泛靶向脂质组 动物全谱代谢组 非靶向代谢组 氧化脂质靶向检测 短链脂肪酸靶向检测 胆汁酸靶向检测 |
|
多 组 学 产 品 |
代谢组+转录组 代谢组+微生物组 代谢组+基因组(mGWAS) 代谢组+蛋白组 |
Tel:027-62433072
网址:www.metware.cn
email:support@metware.cn
创新代谢组及多组学研究领导者
以上是关于重磅综述:人类电生理的脑连接组学的主要内容,如果未能解决你的问题,请参考以下文章